优化MDS患者临床试验设计的策略
时间:2025-04-24 12:12:27 热度:37.1℃ 作者:网络
MDS临床试验设计
骨髓增生异常综合征/肿瘤(MDS)是一种异质性干细胞恶性肿瘤,其特点是预后差,除异基因造血干细胞移植外无治愈性治疗。尽管美国FDA最近批准了一些药物(例如罗特西普、艾伏尼布、地西他滨/cedazuridine和imetelstat),但在开发真正用于治疗MDS患者的变革性疗法方面进展甚微。
推进MDS药物开发的挑战是多方面的,但可以分为特定类别,包括风险分层和临床试验入组标准、反应定义、至事件时间终点、输血终点、功能评估和生物标志物开发。此外,临床试验中过于严格的纳入和排除标准是骨髓增生异常综合征/肿瘤(MDS)患者临床试验入组的诸多障碍之一。许多组织努力提高临床试验资格;然而研究表明,许多MDS患者仍可能被不必要地排除在临床试验之外。
《Blood Advances》近日发表综述,提出了应对这些挑战和优化MDS患者未来临床试验设计的策略,为MDS临床试验的改进提供了有针对性的路线图,旨在优化临床试验设计,加快新药开发。《Blood》也发表了国际骨髓增生异常综合征协会(icMDS)关于MDS临床试验限制性资格标准的立场声明,认为应该避免限制性资格标准,目的是消除临床试验入组的障碍。现整理主要内容供参考。

风险分层和临床试验入组标准
•应收集足够的信息,以便使用ICC或WHO5进行回顾性分类,但应选择一种分类来明确定义研究人群。
•应收集足够的信息,以便使用IPSS-R或IPSS-M进行回顾性预测,但应使用其中一种用于对目标人群进行风险分层。
•在临床试验中尽量减少排除标准和患者入组障碍也至关重要。
反应标准
•在早期反应标准的基础上,根据IWG 2023反应标准收集响应,有助于前瞻性验证。
•在较高危MDS中,具有持久性的CR+PR仍是有临床意义的终点,应得到OS改善的支持。
•在较低危MDS中,符合IWG 2018标准的红系血液学改善数据将允许前瞻性验证。
至事件时间终点
•至事件时间终点应该针对MDS人群,例如疾病风险。
•在较高危MDS中,总生存期仍是至事件时间终点的金标准。可以考虑无事件生存期和无进展生存期,但需要前瞻性验证。
•在较低危MDS中,无输血生存期可作为潜在终点,需要标准定义和前瞻性验证。
•总生存期是所有MDS试验中重要的疗效和安全性终点。
输血终点
•大多数患者可考虑标准血红蛋白输血阈值为7.5-8g/dL。
•入组前16周评估的输血密度可定义低或高输血负担。
•16周或更长时间的TI应认为具有临床意义。
•初步分析应基于意向治疗人群的所有输血,然后进行考虑输血因果关系的敏感性分析。
•考虑“无输血依赖时间”类型的分析。
功能评估和纳入临床试验终点
•在MDS临床试验中纳入预先指定的、全面的患者报告结局终点评估。
•使用定义明确和可靠的工具收集有关合并症、症状、残疾和身体功能的基线数据
•考虑在临床试验设计中使用患者相关因素(例如对于分层因素、入组标准)。
可测量残留病和生物标志物的发展
•同时评估二代测序和流式细胞术用于MRD检测,并保存DNA样本以备将来分析。
•需要常见的疾病反应标准(即IWG 2023的完全缓解)和明确的MRD反应阈值来解释MRD数据并确保试验之间的一致性。
•标准化分析开发并定义分析物测量的最佳灵敏度和特异性。
•考虑在治疗过程中定量记录MRD结果,特别是较高危患者。
•收集针对不同治疗或临床背景的生物标志物(即靶向炎症通路、甲基化或特定靶向突变的治疗)。
icMDS关于消除临床试验入组障碍的建议
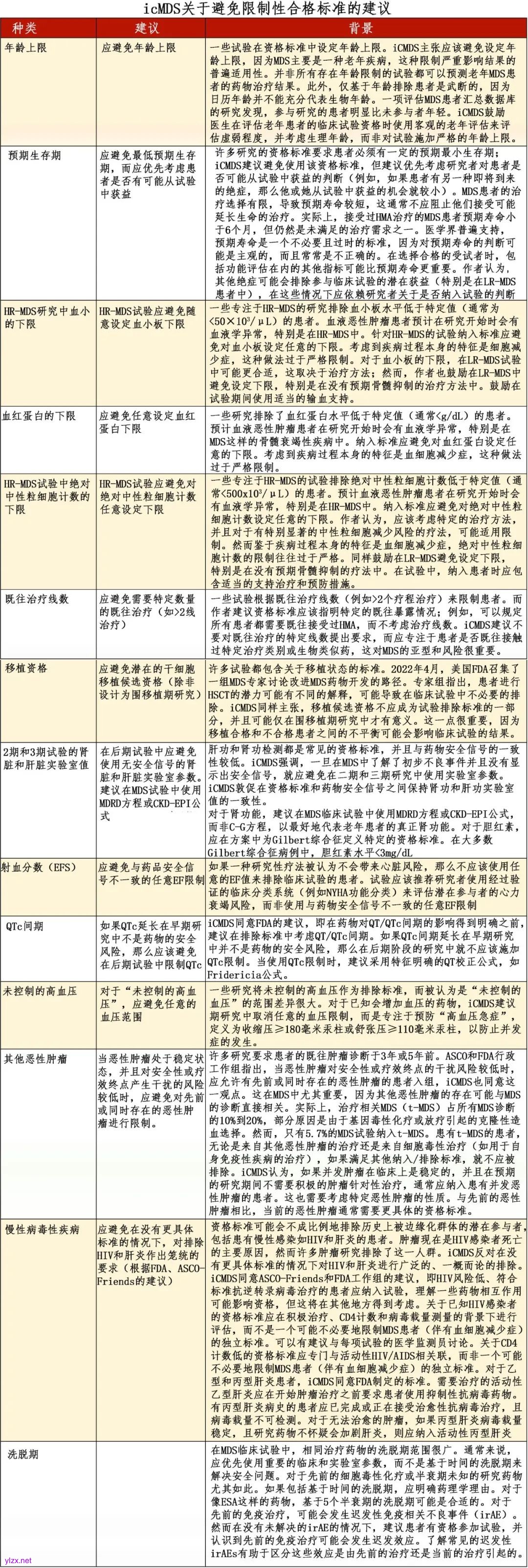
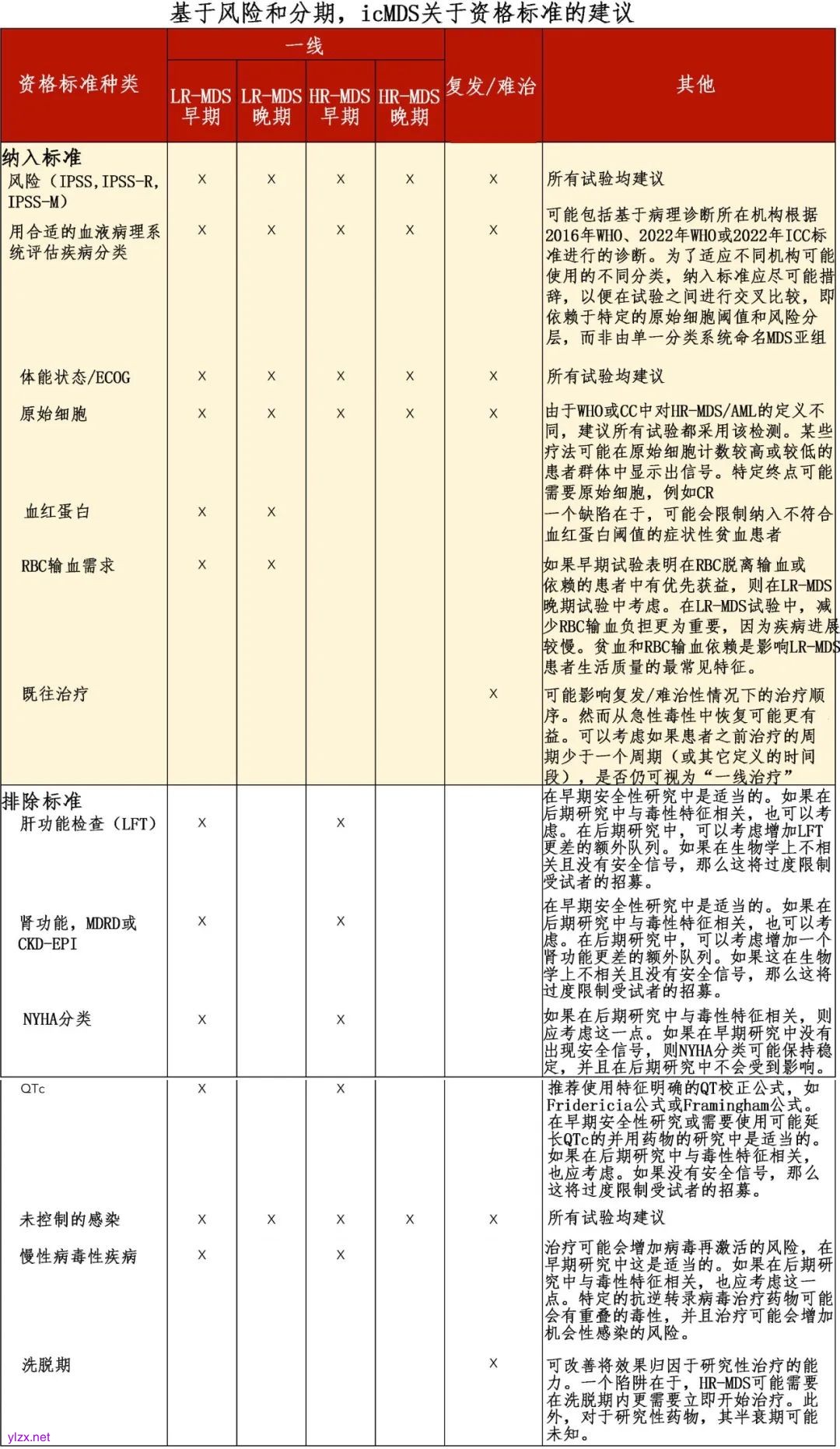
参考文献
Blood Adv . 2025 Mar 11;9(5):1095-1104. doi: 10.1182/bloodadvances.2024014865.
Blood. 2025 Mar 27;145(13):1369-1381. doi: 10.1182/blood.2023023717.


