J Clin Oncol:TAR-200 治疗卡介苗无应答高危非肌层浸润性膀胱癌的疗效与安全性
时间:2025-08-12 12:10:39 热度:37.1℃ 作者:网络
高危非肌层浸润性膀胱癌(NMIBC)患者在接受标准治疗(经尿道膀胱肿瘤切除术联合卡介苗(BCG)膀胱内灌注)后,仍面临较高的疾病复发(12%-60%)或进展(2%-15%)风险,常发展为BCG无应答疾病。目前,根治性膀胱切除术是BCG无应答高危NMIBC的标准治疗方案,但该手术伴随较高的并发症发生率(50%-70%)、90天死亡率(约5%),且严重影响患者生活质量,导致实际临床中接受该手术的患者比例不足20%。
现有FDA批准的治疗方案存在完全缓解(CR)率低、缓解持续时间短、系统或免疫相关毒性明显等问题,且缺乏针对BCG无应答高危乳头状病变仅有的NMIBC的获批治疗方案。此外,传统膀胱内吉西他滨灌注因药物停留时间短,疗效受限。因此,临床亟需安全、有效且能保留膀胱的新型治疗手段。

本研究为IIb期临床试验,旨在评估TAR-200(一种新型膀胱内吉西他滨持续释放系统)单药或联合cetrelimab(PD-1抑制剂)在BCG无应答高危NMIBC患者中的疗效和安全性。具体包括:
-
评估TAR-200单药在BCG无应答的原位癌(CIS)伴或不伴乳头状病变患者中的CR率及缓解持续时间;
-
评估TAR-200单药在BCG无应答的高危乳头状病变仅有的NMIBC患者中的无病生存率(DFS);
-
比较TAR-200单药与TAR-200联合cetrelimab、cetrelimab单药的风险-收益比。
研究设计
本研究为多中心、平行队列的IIb期临床试验,于2021年3月至2024年4月在14个国家的142个中心开展,共纳入4个队列:
-
队列1(C1):53例CIS伴或不伴乳头状病变患者,接受TAR-200联合cetrelimab;
-
队列2(C2):85例CIS伴或不伴乳头状病变患者,接受TAR-200单药;
-
队列3(C3):28例CIS伴或不伴乳头状病变患者,接受cetrelimab单药;
-
队列4(C4):52例高危乳头状病变仅有的患者,接受TAR-200单药。
因中期分析显示TAR-200单药(C2)风险-收益比更优,2023年6月调整方案:关闭C1和C3入组,扩展C2至80例,并新增C4评估乳头状病变仅有的患者。
研究方法
1.患者纳入标准
-
组织学确诊为BCG无应答高危NMIBC(CIS伴或不伴乳头状病变,或高危乳头状病变仅有);
-
距末次BCG治疗≤12个月,且完成足够的BCG治疗(至少5/6剂诱导治疗+2/3剂维持治疗,或至少2/6剂二次诱导治疗);
-
ECOG体能状态0-2分,器官功能良好;
-
拒绝或不适合根治性膀胱切除术。
2.治疗方案
-
TAR-200:通过门诊简短手术植入,前6个月每3周1次,之后至24个月每12周1次;
-
cetrelimab:静脉注射360mg,每3周1次,至18个月;
-
治疗持续至疾病进展、出现不可耐受毒性或完成2年(TAR-200)/18个月(cetrelimab)。
3.评估方法
-
疗效评估:每12周行膀胱镜和尿细胞学检查,每24周行影像检查,24周和48周行膀胱活检;
-
主要终点:C1-C3为中心确认的CR率,C4为DFS率;
-
次要终点:缓解持续时间(DOR)、总生存率、安全性及患者报告结局。
4.统计分析
采用Z检验比较CR率与历史数据(20%),Kaplan-Meier法分析DOR和DFS,安全性分析纳入所有接受至少1剂治疗的患者。
研究结果
1.队列2(CIS伴或不伴乳头状病变,TAR-200单药)
-
CR率:中心确认82.4%(95%CI:72.6-89.8),研究者评估83.5%,两者一致性95.0%;
-
缓解持续性:中位DOR25.8个月(95%CI:8.3-不可估计),52.9%患者DOR≥12个月;
-
安全性:83.5%患者出现治疗相关不良事件(AE),多为低级下尿路症状(尿频43.5%、尿痛40.0%),3级以上AE发生率12.9%,无治疗相关死亡。
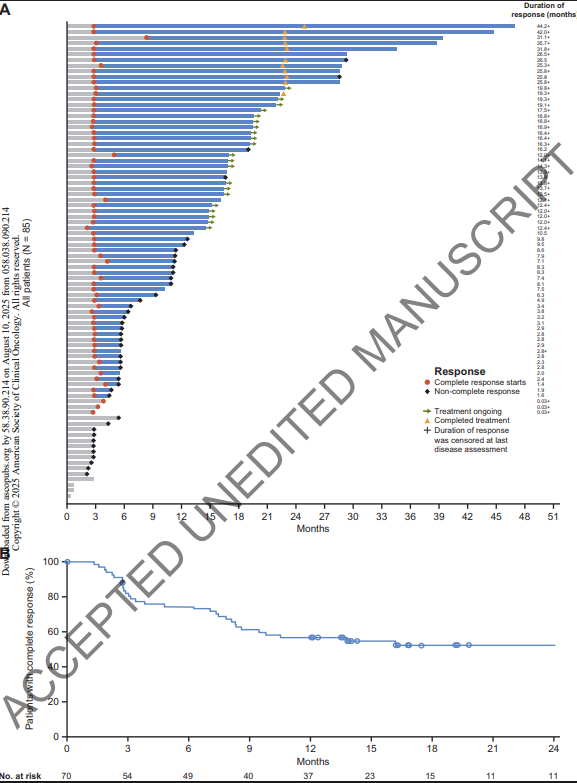
图:TAR-200单药治疗的反应持久性(队列2)
2.队列4(高危乳头状病变仅有,TAR-200单药)
-
DFS率:6个月85.3%(95%CI:71.6-92.7),9个月81.1%(95%CI:66.7-89.7),12个月70.2%(95%CI:51.6-82.8);
-
安全性:80.8%患者出现治疗相关AE,3级以上AE发生率13.5%,主要为膀胱疼痛(3.8%)。
3.队列1和队列3(联合治疗及cetrelimab单药)
-
C1(联合治疗)CR率67.9%,3级以上治疗相关AE发生率37.7%;
-
C3(cetrelimab单药)CR率46.4%,3级以上治疗相关AE发生率7.1%,均低于C2的风险-收益比。
总之,TAR-200单药在BCG无应答高危NMIBC患者中表现出优异的疗效:CIS患者CR率达82.4%,缓解持续时间长达25.8个月;高危乳头状病变仅有患者12个月DFS率70.2%,且安全性良好,主要为可控的低级下尿路症状。与联合治疗或cetrelimab单药相比,TAR-200单药具有更优的风险-收益比,为BCG无应答高危NMIBC提供了一种新型膀胱保留治疗选择。
原始出处
DaneshmandS,VanderHeijdenMS,JacobJM,etal.TAR-200forBacillusCalmette-Guérin–UnresponsiveHigh-RiskNon–Muscle-InvasiveBladderCancer:ResultsFromthePhaseIIbSunRISe-1Study.J Clin Oncol.2025.DOI:10.1200/JCO-25-01651.


