推荐还是限制?25年高血压指南对RDN技术的定位
时间:2025-08-20 12:16:22 热度:37.1℃ 作者:网络
2025年AHA/ACC高血压指南发布后,美敦力等RDN厂商纷纷表示,新版指南进一步确认了RDN(肾动脉去神经术)可作为药物和生活方式干预之外的附加治疗选择,强调RDN可带来持续长达三年的降压效果。
然而,也有一些观点认为,厂家的这些表态更像是在"丧事喜办",指南实际上是对RDN的应用给出了更严格的规范和限制条件,而非真正的积极推荐。
面对当前的争议,我觉得最好的方式就是回到指南原文,看看AHA/ACC的专家委员会到底是怎么表述的,数据究竟支持什么样的结论。
RDN的推荐级别与适应症
核心推荐内容
2025年指南将RDN定位为2b级推荐(可能合理),这个级别其实已经比很多人预期的要高了。 具体推荐是:对于经过仔细筛选的收缩压和舒张压均升高的高血压患者(诊室收缩压140-180 mmHg,舒张压≥90 mmHg),eGFR≥40 mL/min/1.73 m²,在经过优化治疗后仍为难治性高血压,或对额外降压药物治疗产生不可耐受的副作用时,RDN可作为降压药物和生活方式改善的辅助治疗手段。

值得注意的是,指南强调了几个1级推荐的配套要求:所有考虑RDN的患者都应该由具有难治性高血压和RDN专业知识的多学科团队进行评估;同时必须进行充分的医患共同决策,讨论降压的潜在心血管获益与手术风险的对比。

患者选择的具体标准
指南提供了非常明确的患者选择标准。首先是难治性高血压或不可控制的高血压患者:即2级高血压(诊室收缩压≥140 mmHg且舒张压≥90 mmHg)患者,尽管服用≥4种最佳剂量的降压药物(ACEi/ARB + CCB + 噻嗪类利尿剂 + MRA)仍未达标,或者无法耐受最佳剂量的降压药物或额外药物治疗。
💡 笔者提示
很多医生对"难治性高血压"的定义还不够清晰。新版指南特别强调了必须是在排除了假性耐药、白大衣高血压、药物依从性问题和继发性高血压之后才能诊断。实际上,大约20%的"难治性"高血压患者在仔细筛查后会发现是因为服用了升压药物(如NSAIDs)或存在未被发现的继发性高血压。这提醒我们在考虑RDN之前,一定要做足功课。
循证医学证据支撑
关键研究结果分析
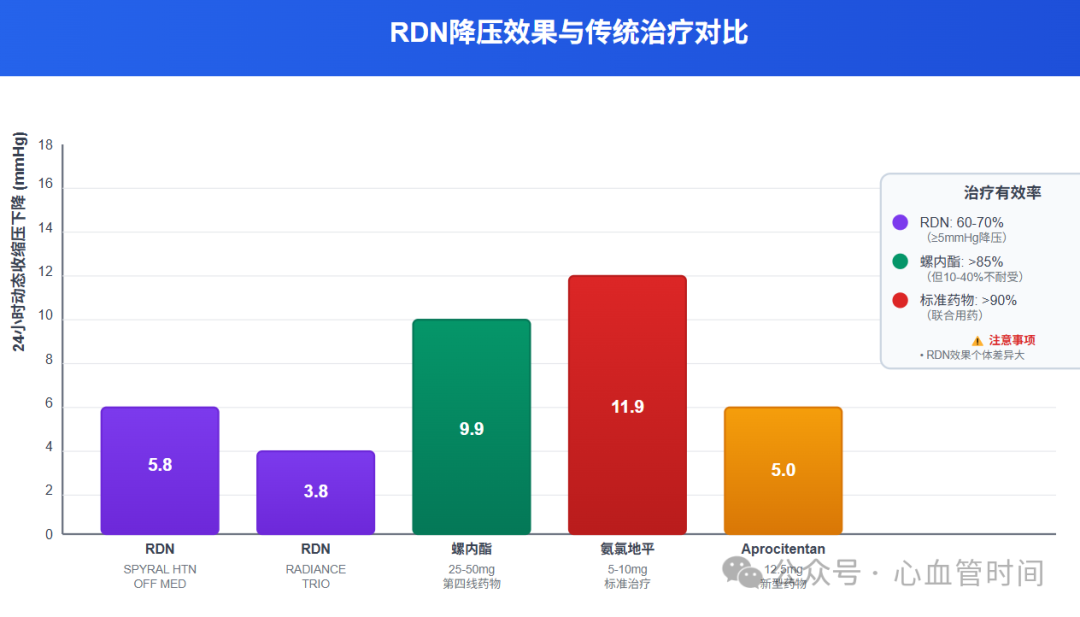
SPYRAL HTN-OFF MED研究作为里程碑式的研究,首次在停药状态下证实了RDN的有效性。该研究显示,在没有服用降压药的情况下,RDN组较假手术组24小时动态收缩压下降4-6 mmHg。这个结果虽然数值不算大,但在没有药物干扰的前提下获得,证据级别相当高。
RADIANCE研究系列(包括RADIANCE-HTN SOLO、RADIANCE II和RADIANCE-HTN TRIO)则进一步验证了RDN在不同药物治疗背景下的效果。特别是RADIANCE-HTN TRIO研究,针对服用三联降压药片仍不达标的患者,RDN组24小时动态收缩压较假手术组额外下降3-5 mmHg。
DENERVHTA研究直接比较了RDN与螺内酯治疗难治性高血压的效果,结果显示RDN的降压效果不优于或相似于螺内酯作为第四种药物。不过这个研究也发现,10%-40%的患者无法耐受螺内酯,这正是RDN可能发挥作用的地方。
💡 笔者提示
从这些研究数据来看,RDN的降压效果确实是适度的,24小时动态收缩压通常下降3-6 mmHg。但需要强调的是,只有60%-70%的患者能够获得有意义的降压效果(≥5 mmHg)。这意味着我们无法预测哪些患者会从RDN中获益,这也是为什么充分的术前讨论如此重要。在我的实践中,我会告诉患者这个技术"不是万能的,但对合适的人可能是救命的"。
操作技术要点与安全性
技术规范与禁忌症
指南明确了RDN的技术要求和禁忌症。所有RDN试验都要求患者的肾动脉直径在3-8 mm之间,而且排除了原有的肾动脉异常,如纤维肌性发育不良、肾动脉狭窄、肾支架植入史和肾动脉瘤等。
绝对禁忌症包括:神经源性体位性低血压、妊娠、纤维肌性发育不良、肾动脉支架植入、肾动脉瘤、显著肾动脉狭窄、已知肾脏或分泌性肾上腺肿瘤。
目前RDN严格通过股动脉入路进行,手术即刻风险与单纯股动脉穿刺的风险相当。但需要注意的是,术后肾动脉狭窄需要干预的风险约为每年0.2%,且在术后前6个月风险最高。
术后监测要求
指南特别强调了术后监测的重要性。由于存在肾动脉狭窄或夹层的风险,建议使用无创影像学检查(如双功能多普勒、CT血管造影或磁共振血管造影)进行术后监测。这个要求在实际工作中不能忽视,因为术后并发症的早期发现和处理直接关系到患者的长期预后。
多学科团队评估的必要性
专业团队配置
新版指南将多学科团队评估列为1级推荐,这反映了RDN并非简单的介入操作,而是需要系统性评估的复杂医疗决策。理想的团队应包括:具有继发性高血压筛查专业知识的高血压专科医生,以及具有充分培训和处理手术并发症能力的介入医生。
评估过程必须包括24小时动态血压监测和直立位生命体征测量,同时要筛查继发性高血压。这是因为大多数RDN试验都将可直接治疗的继发性高血压、白大衣高血压和伴有体位性低血压的仰卧位高血压作为排除标准。
💡 笔者提示
多学科评估确实发现了不少问题。有些患者在转介过来时被认为是"难治性"高血压,但经过仔细评估后发现是原发性醛固酮增多症或睡眠呼吸暂停综合征。这种情况下,针对病因的治疗显然比RDN更有意义。我建议在考虑RDN之前,一定要有心内科、肾内科和内分泌科的联合会诊,确保没有遗漏可治疗的继发性原因。
与传统治疗的比较
RDN vs 螺内酯
指南特别提到了RDN与螺内酯(第四线药物)的比较。虽然多数情况下螺内酯的降压效果不劣于RDN,但螺内酯的不良反应(特别是男性乳房发育、高钾血症)确实限制了部分患者的使用。这为RDN在特定患者群体中的应用提供了合理性。
在慢性肾病患者中,非甾体MRA治疗难治性高血压的证据有限,需要密切监测血钾。而RDN的eGFR门槛设在40 mL/min/1.73 m²以上,这意味着对于中重度慢性肾病患者,我们仍需要更多证据。
其他替代治疗选择
当螺内酯或依普利酮因副作用或费用问题无法使用时,阿米洛利(10-20 mg)已被证明与螺内酯同样有效。其他替代的四线和五线药物还包括β受体阻滞剂、α受体阻滞剂、中枢交感抑制剂和直接血管扩张剂。
值得一提的是,双重内皮素受体拮抗剂阿洛西坦(aprocitentan)在难治性高血压患者中显示出4-6 mmHg的24小时动态收缩压下降效果,但腿部水肿和液体潴留的副作用(9%-18%)可能限制其在某些患者中的应用。这个药物目前尚未在国内上市,但作为了解国际前沿进展还是很有价值的。
临床决策的实用建议
患者筛选流程
基于指南推荐和临床经验,我建议采用以下筛选流程:
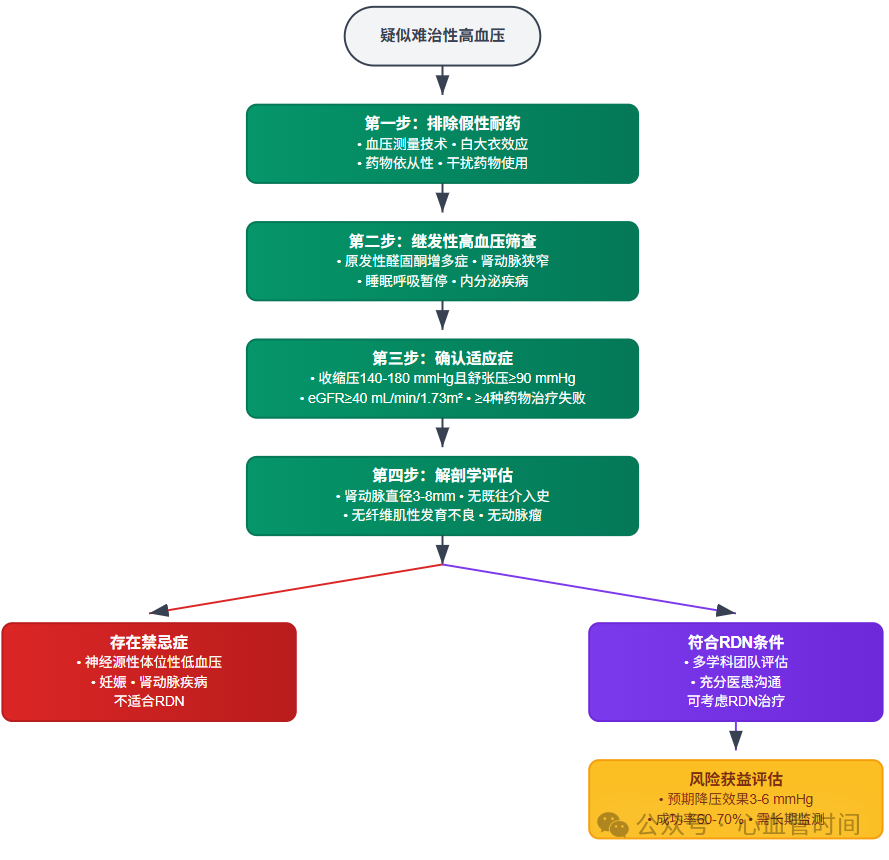
首先确认真正的难治性高血压,这包括排除假性耐药(测量技术、白大衣效应)、药物依从性问题和干扰药物使用。然后进行系统的继发性高血压筛查,特别关注原发性醛固酮增多症、肾动脉狭窄和睡眠呼吸暂停。
接下来评估患者是否符合解剖学标准:肾动脉直径3-8 mm,无既往肾动脉介入史,无纤维肌性发育不良等。最后评估患者的整体风险获益比,包括预期寿命、手术风险和对血压控制的迫切程度。
💡 笔者提示
实际工作中,我遇到过一些患者强烈要求RDN,认为这是"根治高血压"的方法。这时候医患沟通就特别重要。我会明确告诉患者,RDN不是高血压的治愈性治疗,也不能完全替代药物治疗。大多数患者术后仍需要继续服用降压药,只是可能会减少用药种类或剂量。设定正确的期望值是成功治疗的前提。
术后管理策略
RDN术后的管理同样重要。除了前面提到的影像学监测外,血压管理也需要调整策略。由于RDN的效果通常在术后2-3个月才能完全显现,术后早期不建议贸然减药。
建议在术后1个月、3个月、6个月和1年进行规律随访,监测血压变化、肾功能和可能的血管并发症。如果6个月后血压仍无明显改善,需要重新评估治疗策略,可能需要调整药物治疗或考虑其他干预措施。
争议与局限性
当前争议点
尽管指南给出了明确推荐,但RDN仍存在一些争议。首先是降压效果的预测性问题:目前还没有可靠的生物标志物能预测哪些患者会从RDN中获益。这种"碰运气"的感觉确实让一些医生和患者感到不安。
其次是长期安全性数据的缺乏。虽然短期(2-3年)的安全性数据相对令人放心,但RDN对肾功能的长期影响、以及肾动脉再狭窄的远期风险仍需要更长时间的观察。
适应症扩展的可能性
FDA批准的RDN设备适应症实际上比指南推荐的更广泛,这也反映了监管部门与学术界在证据解读上的微妙差异。未来可能的适应症扩展方向包括:单纯收缩期高血压、进展期慢性肾病患者、以及某些继发性高血压(如原发性醛固酮增多症)的辅助治疗。
不过在这些新适应症有充分证据支持之前,我们还是应该严格按照指南推荐的标准来选择患者。
总结
2025年高血压指南对RDN的推荐标志着这项技术从实验性治疗向临床规范化应用的重要转变。虽然推荐级别仍然谨慎(2b级),但明确的适应症、禁忌症和操作规范为临床实践提供了有力指导。
关键要点包括:RDN仅适用于经过严格筛选的难治性高血压患者,降压效果适度但持续,必须由多学科团队评估,充分的医患沟通不可或缺,术后长期监测必须跟上。对于那些真正无法耐受多种降压药物副作用的患者来说,RDN确实提供了一个有价值的治疗选择。
在可预见的未来,药物治疗仍将是高血压管理的基石,而RDN则为那些特殊情况下的患者提供了额外的希望。


