乳腺癌开放全乳切除术后胸大肌前与胸大肌后双平面假体联合补片即刻乳房重建效果的前瞻性队列研究
时间:2025-08-20 12:17:41 热度:37.1℃ 作者:网络
摘 要
目的 对比乳腺癌开放全乳切除术后胸大肌前(prepectoral breast reconstruction,PBR)与胸大肌后双平面(subpectoral dual-plane breast reconstruction,SBR)假体联合补片即刻乳房重建患者的满意度与安全性。方法 通过前瞻性队列研究,对2021年6月—2022年10月于四川大学华西医院行开放全乳切除术后PBR或SBR假体联合补片即刻乳房重建乳腺癌患者的临床资料进行分析。根据乳房重建方式,将患者分为PBR组和SBR组。比较两组患者在术后第1、3、7、14天的疼痛评分和术后14 d内镇痛药物的使用情况及随访期内术后并发症、乳房满意度和生活质量的差异。结果 共纳入62例女性患者,其中PBR组35例,平均年龄(39.6±6.5)岁,SBR组27例,平均年龄(41.5±9.9)岁。SBR组患者在术后第3天(P=0.032)、第7天(P<0.001)、第14天(P<0.001)的疼痛评分显著高于PBR组,且在术后14 d内使用镇痛药物患者比例更高(P=0.001)。PBR组中位随访时间28.4个月,SBR组中位随访时间34.9个月,两组患者在随访期内的外科总并发症(P=0.583)、主要并发症(P=0.526)及次要并发症(P=0.532)发生率差异均无统计学意义。PBR组共有1例(2.9%)、SBR组共有2例(7.4%)患者植入物丢失(P=0.575)。SBR组运动畸形及胸部肌肉疼痛患者各4例,而PBR组没有患者出现运动畸形或胸部肌肉疼痛(P=0.031)。PBR组和SBR组分别有5例(14.3%)、11例(40.7%)患者出现包膜挛缩(P=0.023)。PBR组波纹征(25.7% vs. 3.7%,P=0.047)、假体轮廓显现(40.0% vs. 11.1%,P=0.020)发生率显著高于SBR组。术后24个月,PBR组患者的乳房满意度[(67.9±13.1)分vs.(52.6±16.9)分,P=0.025]及胸部功能满意度[(70.7±13.4)分vs.(58.7±14.3)分,P=0.035]更高。PBR组患者在随访期内均未发生肿瘤的局部复发、远处转移及死亡,SBR组有1例患者发生肿瘤的局部复发及远处转移,无患者死亡。结论 与SBR相比,PBR更符合乳房的生理解剖层次,有效避免了术后运动畸形和胸部肌肉疼痛,包膜挛缩发生率更低,术后乳房满意度和胸部功能满意度更高,是一种安全可行的重建方法,对一些特定患者,尤其是有较高运动需求的患者,是一种更佳的重建选择。
正 文
对于早期乳腺癌患者,保乳手术(breast conservative therapy,BCT)是首选[1-2]。我国BCT比例不足20%[3]。全乳切除给患者身心带来负面影响[4]。乳房重建能改善身体形象和生活质量[5-7],其中基于植入物的乳房重建(implant-based breast reconstruction,IBBR)最常见[8-9]。最初,假体置于胸大肌前,但因高并发症发生率[10-11],该术式被放弃。后改为胸大肌后放置假体(全胸肌后乳房重建),这种术式限制了假体的大小,术后易出现双乳不对称,尤其是对于45~55岁患者[12],乳房下垂十分普遍[13-14],双平面乳房重建可以实现一定的乳房下垂度[15-16],但未完全解决运动畸形与胸大肌疼痛,且术后易发生乳房变形。部分外科医师[17-19]尝试用补片覆盖假体置于胸大肌前以改善美学效果,但有研究[20-21]指出该方法可能增加并发症风险。目前,关于假体最佳放置平面的选择仍存在争议。现有研究多关注脱细胞真皮基质(acellular dermal matrix,ADM),ADM较厚但感染风险较高[22],TiLoop Bra®(钛化物聚丙烯修补网)具有较低成本和较薄结构[23],并逐渐应用于乳房重建。关于TiLoop Bra®联合假体的即刻乳房重建与胸大肌前后双平面放置假体的效果,2014年Casella等[24]报道了一项相关研究,但未涉及美学效果差异。
1 资料与方法
1.1 临床资料和分组
前瞻性纳入2021年6月—2022年10月拟于四川大学华西医院行开放全乳切除术后假体联合补片即刻乳房重建的乳腺癌患者。根据患者肿瘤学信息、乳房外形及大小、身形及患者自己意愿等制定手术方案并分别入组,包括胸大肌前乳房重建(prepectoral breast reconstruction,PBR)组和胸大肌后双平面乳房重建(subpectoral dual-plane breast reconstruction,SBR)组。
纳入标准:(1)年龄≥18岁;(2)女性;(3)术前穿刺或切除病理证实为乳腺癌;(4)多中心性病灶、广泛的导管内病变、单灶肿瘤较大而不适合行保乳手术;(5)肿瘤未侵及皮肤、皮下组织以及胸大肌,无远处转移。排除标准:(1)乳房有明显下垂(超过Ⅱ度下垂),需要运用Wise-pattern或其他乳房提升法进行皮下乳房腺体切除;(2)既往乳腺癌病史(同侧BCT后复发);(3)双侧乳腺癌;(4)病情危重,难以对手术的有效性和安全性做出确切评价;(5)正在参加其他临床试验,可能会对本试验造成影响。
新辅助化疗不是不保留或保留乳头乳晕复合体的乳房皮下切除术和IBBR的禁忌[25],因此经纳排标准筛选后的新辅助化疗患者也被纳入该研究。
1.2 手术方法
根据患者入组情况分别进行手术,本研究所涉及的手术共由5个医疗组/5名外科医师分别完成,切口根据主刀医师经验可选择经乳晕切口、下皱襞切口或放射状切口。游离皮瓣范围上达锁骨下方,内达胸骨边缘,下达肋弓处,外侧达背阔肌前缘。
1.2.1 PBR组假体放置方法
补片预先植入患侧皮瓣下胸大肌前方,并将其上缘与胸大肌表面缝合固定,与胸大肌共同形成半开放的袋状空间,即假体腔,由补片构成假体腔前壁,于假体腔内置入假体,使假体前方由补片覆盖,后方由胸大肌衬垫,将补片下缘与胸大肌表面缝合封闭假体腔的下外侧缘。PBR组详细的手术体位、腋窝手术及皮下腺体切除、补片缝合及假体植入、术后护理等信息在我们的既往研究[26]中有所描述。
1.2.2 SBR组假体放置方法
游离患侧胸大肌深面后,于胸大肌下方胸壁附着点处切断其内下和内侧部分肌肉,1000 mL蒸馏水相继冲洗各创腔。胸大肌断端下缘与补片上缘连续缝合形成双平面覆盖假体表面,使假体的下半部分及外侧部分由胸大肌及补片覆盖。除补片缝合及假体植入与PBR组不同外,SBR组的手术体位、腋窝手术及皮下腺体切除、术后护理等与PBR组相同。
1.3 美容效果、生活质量、安全性及术后疼痛评估
研究团队的外科医师或医学生(回避本人参与的手术)将对本研究结果进行评估。术前详细收集患者的人口学、肿瘤学及其他相关资料,患者需填写术前BREAST-Q量表,包括乳房满意度、社会心理健康、性生活满意度、胸部功能满意度,术中记录患者手术方式、手术切口、植入假体的大小等。研究者团队与每例患者均添加联系方式,提醒患者在术后不同随访时间点返回门诊免挂号进行随访以增加随访配合度。患者需要于术后2周、1个月、3个月、6个月、1年、2年至门诊随访,客观记录术后并发症,于术后24个月填写BREAST-Q量表。而对于外地不便至门诊随访的患者,通过微信或电话指导其填写电子问卷,再由研究团队统计转换分数。对于并发症的评估,除电话详细询问外,患者自愿拍摄不露脸的乳房照片用于评估。而拒绝拍摄乳房照片的患者仅完成电子问卷及电话随访并发症。
1.3.1 美容效果及生活质量评估
采用BREAST-Q乳房重建模块问卷对两组患者术前、术后的乳房满意度、社会心理健康、性生活满意度、胸部功能满意度进行评估。将患者的原始比例总分转换为从0(最差)到100(最好)的分数,分数越高提示结果越好。BREAST-Q问卷于2009年发布[27],至今仍是评估乳房手术患者满意度的金标准。
1.3.2 安全性评估
采用Clavien-Dindo分级法(Clavien-Dindo classification,CDC)进行外科并发症的分类[28]。次要并发症定义为Ⅰ~Ⅱ级并发症,主要并发症定义为Ⅲ级(需要手术、内镜或放射干预)或Ⅳ级(危及生命)并发症。植入物相关并发症指重建术后与植入物相关的影响患者乳房美观度及生活质量的并发症,如胸大肌离断导致的运动畸形、胸大肌疼痛、包膜挛缩、波纹征及假体轮廓显现等。包膜挛缩根据Baker分级进行定义[29]。并发症的发生和治疗通常未纳入BakerⅠ级和Ⅱ级包膜挛缩[30-31],因此,在本研究中,只有BakerⅢ级及Ⅳ级包膜挛缩才被纳入植入物相关并发症的统计。我们根据手术切缘阳性率、局部复发、远处转移和总生存期评估肿瘤结局。局部复发定义为累及同侧乳房、胸壁或区域淋巴结。
1.3.3 术后疼痛评估
采用数字疼痛评分量表(numerical pain rating scale,NPRS)于术后第1、3、7、14天早晨使用镇痛药物前指导患者从0(无疼痛)到10(可以想象到的最严重疼痛)对患侧乳房、胸部疼痛情况评分。
1.4 统计学分析
采用SPSS 25.0软件对所有数据进行分析。非正态分布的计量资料用中位数(范围)表示,组间比较采用Mann-Whitney U检验;正态分布计量资料用均数±标准差(x±s)表示,组间比较采用独立样本t检验。采用重复测量方差分析比较两组患者术后不同时间点的疼痛评分变化趋势,若满足球形假设,则根据主体内效应检验分析结果,若不满足球形假设,则通过多变量检验分析结果。计数资料采用频数和百分比表示,组间比较采用χ2检验或Fisher确切概率法,等级资料的比较采用秩和检验。双侧检验水准α=0.05。
1.5 伦理审查与临床试验注册
该前瞻性队列研究严格遵守赫尔辛基宣言(2013版),研究数据来源于一项对比日间与住院部乳腺手术的全国多中心前瞻性研究,该研究经四川大学华西医院生物医学伦理审查委员会批准,批准号:2021年审(592)号;并在中国临床试验注册中心(clinicaltrials.gov)注册,注册号:ChiCTR2100047081。
2 结果
2.1 患者基线和手术资料
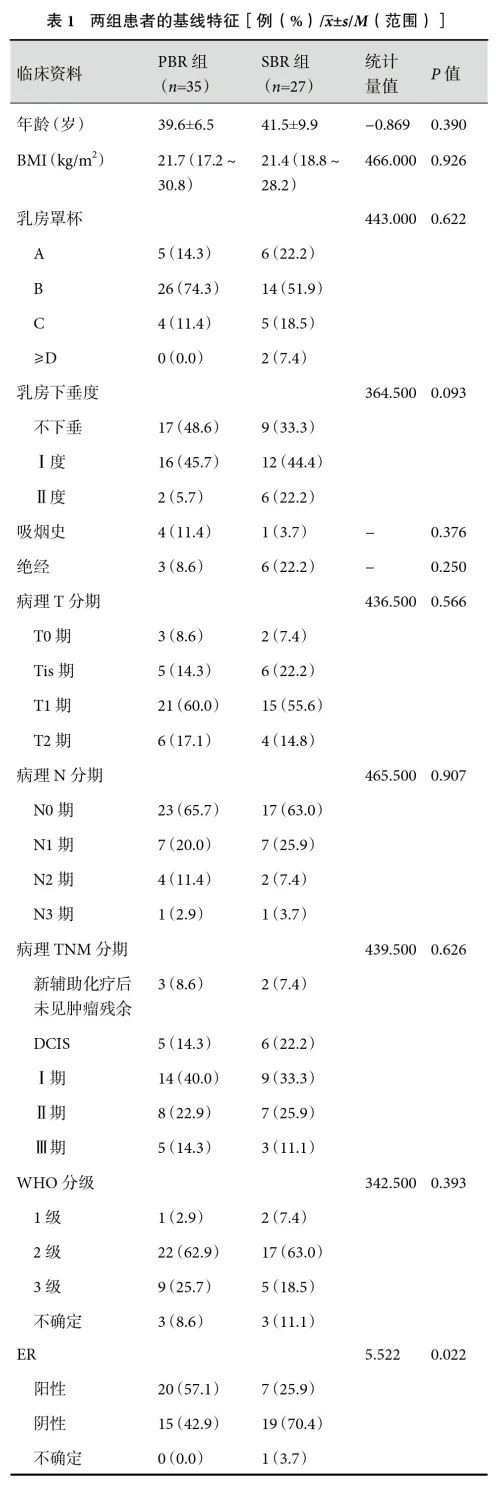
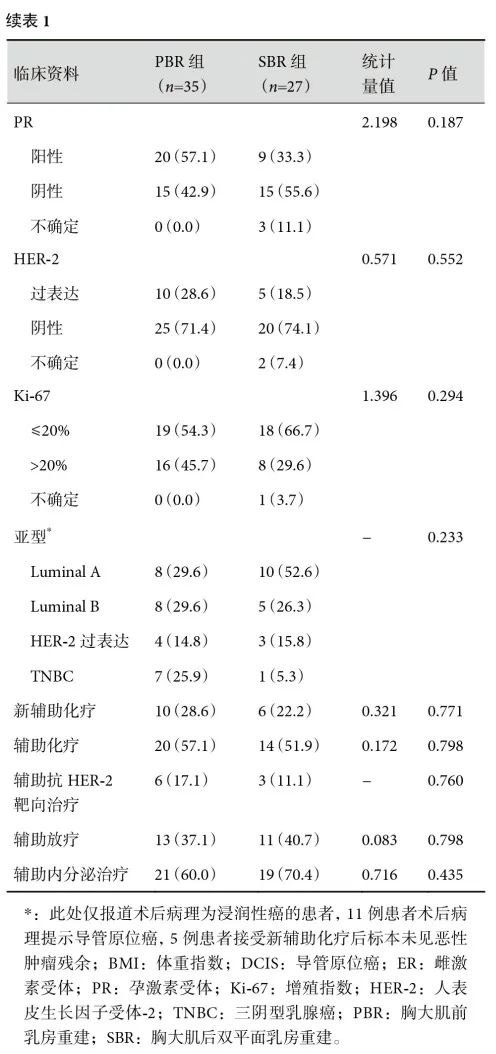
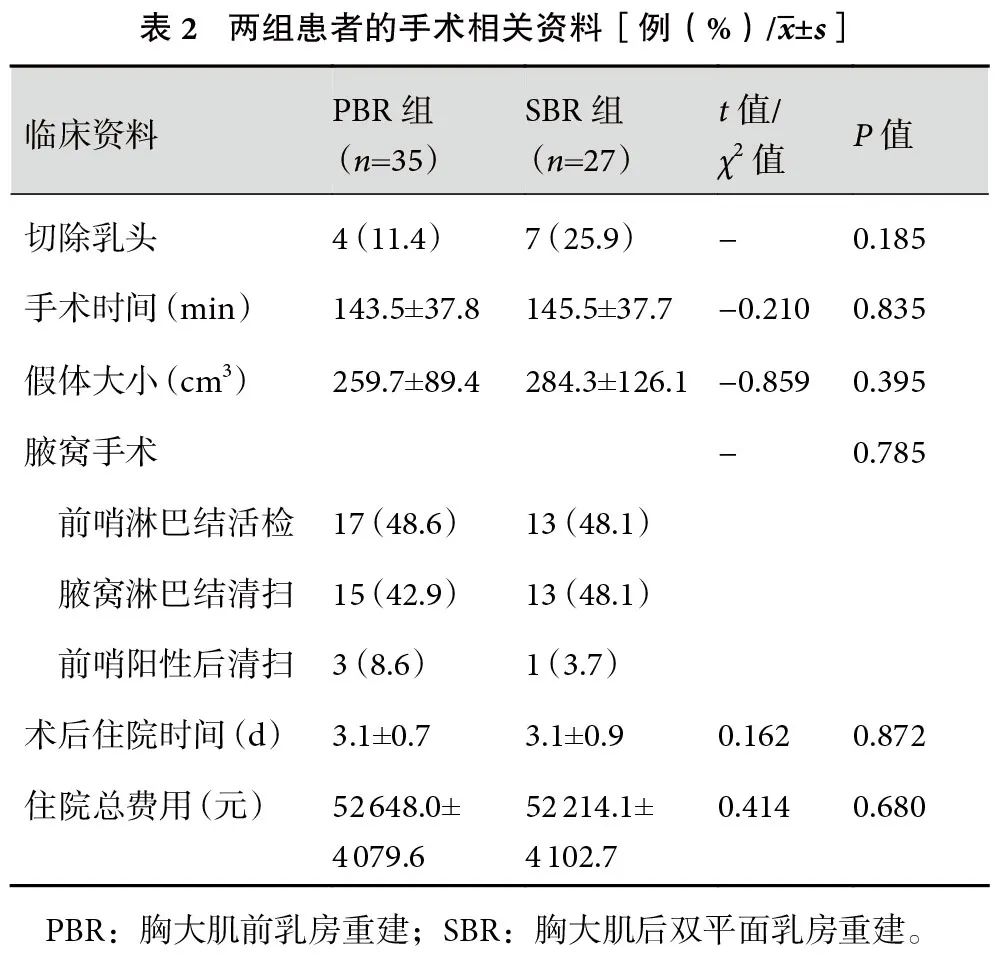
研究共纳入62例患者(62个乳房),其中PBR组35例,SBR组27例。两组患者的雌激素受体(P=0.022)差异有统计学意义,其他基线资料差异无统计学意义(P>0.05);见表1。两组患者的手术资料差异无统计学意义(P>0.05);见表2。
2.2 随访结果
PBR组患者中位随访时间28.4个月,SBR组患者中位随访时间34.9个月,随访率100.0%。重复测量方差分析结果提示,62例患者的术后疼痛评分均随着时间的推移逐渐下降(P<0.001),且组间差异有统计学意义(P=0.003)。两组患者在术后第1天的疼痛评分差异无统计学意义[(5.8±1.3)分vs.(5.8±1.2)分,B=−0.006,P=0.984],然而SBR组患者在术后第3天[(3.5±1.7)分vs.(4.3±1.1)分,B=−0.790,P=0.032]、第7天[(1.9±1.5)分vs.(3.4±1.6)分,B=−1.550,P<0.001]、第14天[(1.0±1.2)分vs.(2.3±1.3)分,B=−1.325,P<0.001]的疼痛评分均显著高于PBR组。PBR组患者术后镇痛药物的使用率为5.7%,SBR组的使用率达40.7%,差异有统计学意义(P=0.001)。
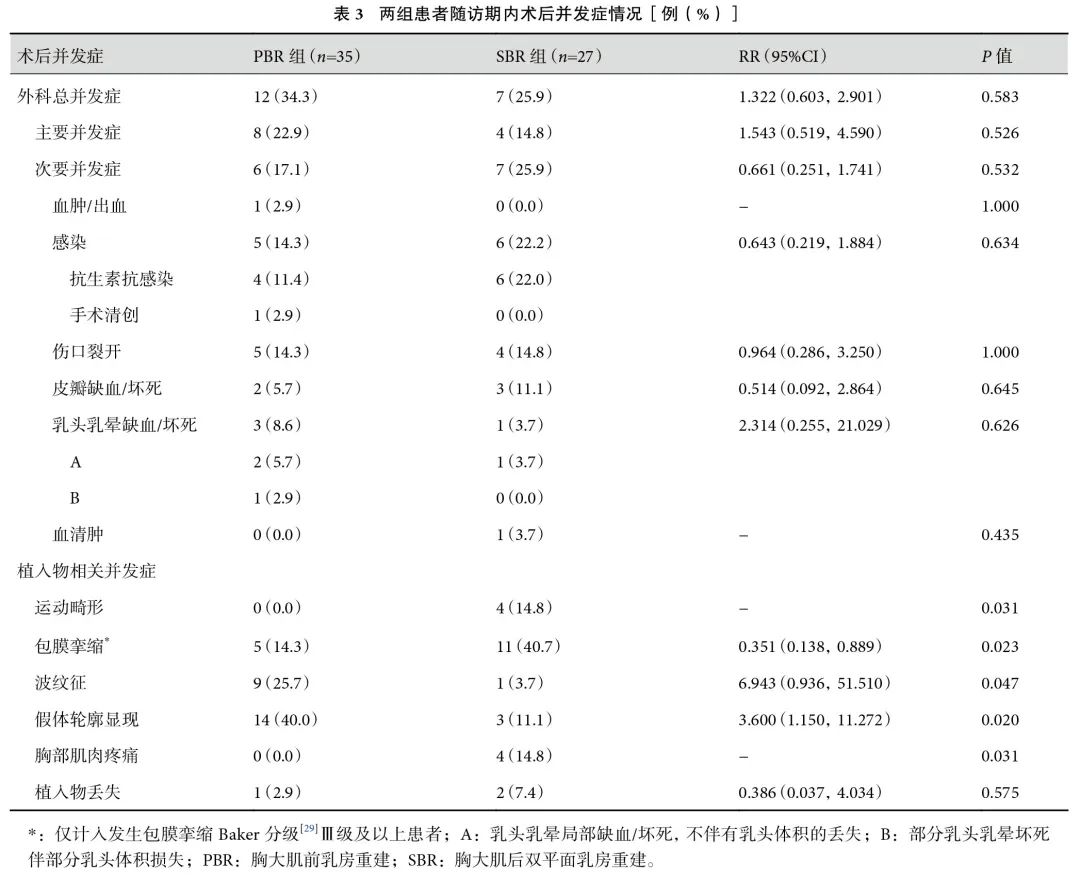
本研究将术后并发症分为外科并发症、植入物相关并发症。在随访期内,PBR组的外科总并发症发生率为34.3%,其中主要并发症发生率为22.9%,次要并发症发生率为17.1%;SBR组的外科总并发症发生率为25.9%,其中主要并发症发生率为14.8%,次要并发症发生率为25.9%,两组患者在随访期内的外科总并发症、主要并发症、次要并发症差异均无统计学意义(P>0.05)。但SBR组运动畸形(P=0.031)、包膜挛缩(P=0.023)、胸部肌肉疼痛(P=0.031)并发症发生率更高,PBR组波纹征(P=0.047)、假体轮廓显现(P=0.020)发生率更高;见表3。
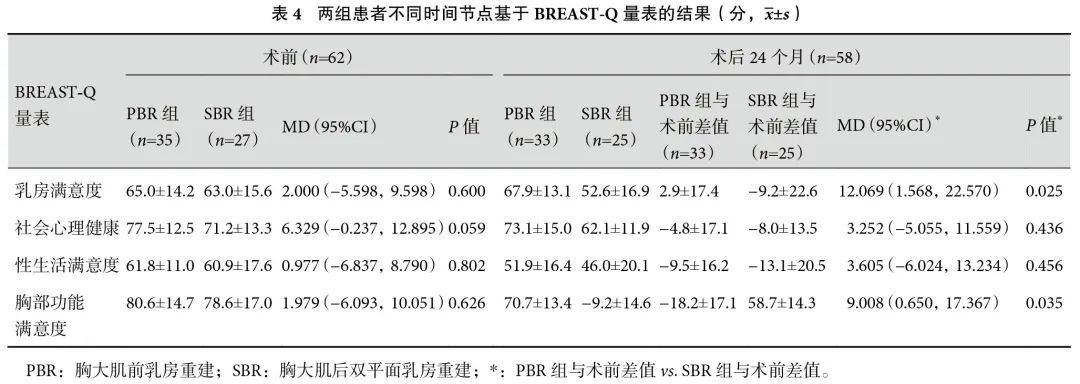
62例患者均完成术前BREAST-Q问卷,58例患者完成术后24个月的BREAST-Q问卷,两组患者术前BREAST-Q量表结果差异无统计学意义(P>0.05)。术后24个月,PBR组的乳房满意度(P=0.025)、胸部功能满意度(P=0.035)显著高于SBR组,然而两组患者的社会心理健康(P=0.436)、性生活满意度(P=0.456)差异无统计学意义;见表4。
PBR组患者在随访期内均未发生肿瘤局部复发、远处转移及死亡,SBR组有1例患者在术后29.4个月发生肿瘤局部复发(同侧腋窝淋巴结转移)及远处转移(肝、骨转移),无患者死亡。
3 讨论
本研究是使用TiLoop Bra®前瞻性对比分析PBR与SBR患者满意度和安全性的第一项研究。本研究发现,PBR和SBR在随访期内的外科学安全性相似,而PBR在术后24个月呈现出更好的乳房满意度,同时PBR能够减少手术创伤,降低术后疼痛评分,也能够明显改善SBR伴随的植入物相关并发症,如运动畸形、包膜挛缩、胸部肌肉疼痛。
PBR避免了胸大肌的离断,减少了手术创伤,相较于SBR,患者能更快地恢复生活和工作。本研究分析了两组患者不同时间点的术后疼痛评分,两组患者术后第1天的疼痛评分没有显示出差异,我们认为是术后正常的疼痛反应和全身麻醉药物的影响。但随着时间的推移,PBR组患者的术后疼痛评分更低,并且更少使用镇痛药物,我们认为术后急性期的疼痛和胸大肌的离断有关。此外,本研究发现PBR组随访期内胸部肌肉疼痛发生率更低,术后24个月的胸部功能满意度更高。我们认为慢性期的疼痛和假体置于胸大肌后,对胸大肌产生明显的压迫症状,胸大肌长时间处于过度拉伸状态,运动过程中假体和胸大肌的起点发生摩擦,因此SBR组患者在术后长时间内可能会有胸部肌肉疼痛、胸部紧绷牵扯感、疼痛过敏等不适。上述结果提示接受PBR患者术后可能具有更好的胸部功能。在之前发表的研究[26]中,我们推测PBR可能缩短了手术时间,然而在本研究中,尽管PBR组的平均手术时间短于SBR组,但差异无统计学意义,可能是由于研究样本量较小,以及研究开始时处于PBR学习曲线的初期阶段。
关于术后安全性的对比,我们将术后并发症分为外科并发症、植入物相关并发症分别阐述。两组患者在外科总并发症、主要并发症及次要并发症发生率上均未见统计学差异,这与Ng等[32]的回顾性研究结果一致。由于PBR将假体直接置于皮下,没有胸大肌作为血供的补偿,可能增加切口裂开、乳头乳晕坏死、皮瓣坏死的发生风险。本研究中,我们发现PBR组的外科主要并发症发生率呈现更高的趋势,合并后分析我们发现两组患者的外科总并发症发生率差异无统计学意义,表明PBR是安全的。尽管本研究两组患者均报道了较高的外科并发症发生率,但我们对并发症的评估均按照CDC标准进行,CDC标准相较于其他并发症评估标准更为严格。PBR组在植入物相关并发症的发生率上表现出显著的优势,尤其是消除了运动畸形和胸部肌肉疼痛。在SBR组,假体由胸大肌覆盖,当涉及需要胸大肌收缩的动作时,如俯卧撑、卧推等,胸大肌挤压假体,外观上表现为重建乳房的乳头乳晕位移,表面皮肤的皱褶,整个重建乳房的位移,通常伴随胸部肌肉疼痛[33]。此外,SBR组的包膜挛缩率显著高于PBR组。Liu等[34]通过回顾性研究报道了类似的结果,且包膜挛缩发生率在放疗患者中更高[35]。≥Ⅲ级包膜挛缩不仅会影响术后重建乳房的美学效果,还会给患者带来不适感,这也是一些患者选择二次或多次手术调整的主要原因[36]。另一方面,不同于SBR具有富血管化的肌肉层覆盖,PBR将假体直接置于皮下,尽管假体表面有补片覆盖,但其波纹征、假体轮廓显现的发生率仍显著高于SBR组。两组患者在植入物丢失方面无显著差异,PBR组的1例患者在术后18个月无明显诱因发生感染化脓导致的假体丢失,SBR组的2例患者分别在术后3个月因切口裂开导致假体外露继而假体丢失、在术后6个月因皮瓣缺血坏死致假体丢失。PBR组患者在随访期内未发生肿瘤的局部复发和远处转移。综上所述,PBR未增加术后外科并发症的发生风险,同时具有降低运动畸形、包膜挛缩、胸部肌肉疼痛发生率的优势,对于有较高运动需求的女性患者,PBR可能是更佳的选择。然而,PBR的缺点在于波纹征、假体轮廓显现的发生率更高,因此根据患者的不同需求选择重建方式尤为重要。
PBR将假体置于胸大肌前方,位置和乳腺的生理解剖层次相同,患者术后具有更高的乳房满意度。本研究中,PBR组在术后24个月的乳房满意度较SBR组更高,可能是由于SBR组急性变形期(术后早期出现因全身麻醉肌肉松弛药物作用解除后胸大肌收缩引起的皮肤、乳头乳晕和假体移位,从而出现双侧不对称的高低胸)的影响,以及慢性变形期(后期由于胸大肌的失用性萎缩还会再次带动皮肤、乳头乳晕和假体上移,影响乳房外形,尤其对于术后接受放疗的患者更是如此)在后期逐渐表现出来的结果,这与Reitsamer等[37]的研究结果一致。两组患者术后24个月的性生活满意度无明显差异,并且均低于术前水平,可能是由于重建的乳房无法达到和健侧乳房完全对称,尤其是对于大而下垂乳房的患者,下垂度的差异于患者站立位时更加明显,凸度的差异于患者平卧位时更加明显。此外,重建患者术后乳房感觉麻木,也可能是影响性生活满意度的重要因素。但PBR组患者术后与术前性生活满意度差异较SBR组更小。关于社会心理健康,两组患者在术后24个月未达到术前水平,术后社会心理健康水平的降低可能是与疾病本身有关,但PBR组术后与术前差异较SBR组更小,我们认为可能与PBR组患者对自身乳房更满意,社交更自信,认可自己的身材有关。两组患者在社会心理健康、性生活满意度上的差异可能需要更大的样本量、更长时间随访得以体现。
本研究报道了两组患者的中期随访结果,但仍然存在局限性,如未能统计患者使用镇痛药物的种类及频次,只要患者使用过镇痛药物即被记录为使用了镇痛药物;研究样本量较小以及非随机化的研究设计;某些并发症,如包膜挛缩、假体轮廓显现、波纹征等,随着随访时间的延长发生率可能更高;本队列也未报道两组患者最终的美学效果。需要更大样本量、更长随访时间、多中心随机对照研究进一步证实。
综上所述,与SBR相比,PBR更符合乳房的生理解剖层次,有效避免了术后运动畸形和胸部肌肉疼痛,包膜挛缩发生率更低,拥有更高的术后乳房满意度和胸部功能满意度,是一种安全可行的重建方法。对一些特定患者,尤其是有较高运动需求患者,PBR是一种更佳的重建选择。
利益冲突:无。
作者贡献:肖晓负责实施研究,撰写文章;朱中建负责修改论文;冯玉、周娇、周云负责资料采集,文献解读;杜正贵负责研究方案制定及设计,指导研究。


