《应用人工智能改善心脏病临床结局:美国心脏协会科学声明》解读
时间:2025-08-25 12:14:23 热度:37.1℃ 作者:网络
摘 要
当前,学术界、工业界及各国政府机构均致力于开发并应用人工智能及其他先进分析工具,以推动医疗服务的变革。然而,目前仍存在诸多挑战,仅有少数人工智能工具在改善心血管疾病与卒中临床结局方面取得了足够的成效并被广泛应用。为此,美国心脏协会制定了相关科学声明,概述了人工智能算法与数据科学在心血管疾病诊断、分类及治疗中的最新研究进展,并总结了目前人工智能工具的最佳实践模式、研究空白及现存挑战,旨在推动该领域的发展。本文结合笔者团队的相关研究实践,对此科学声明进行解读
正 文
人工智能(artificial intelligence,AI)算法工具的应用正受到学术界、工业界及各国政府机构的广泛推动,各方均投入大量资源,致力于利用AI技术革新医疗保健服务。这一趋势促使过去10年间与医疗保健相关的AI研究论文数量迅速增长,并预计在未来几年内将进一步加速发展。目前,AI相关研究已广泛应用于多个临床场景,包括对电子健康记录(electronic health records,EHR)的数字化分析,以探讨治疗效果的异质性、诊断检测与干预措施的有效性[1]。近年来,该领域研究进一步拓展至预测模型[2]、分类模型的构建[3]及临床随机试验设计[4],以提升临床决策的精准性(图1[5])。
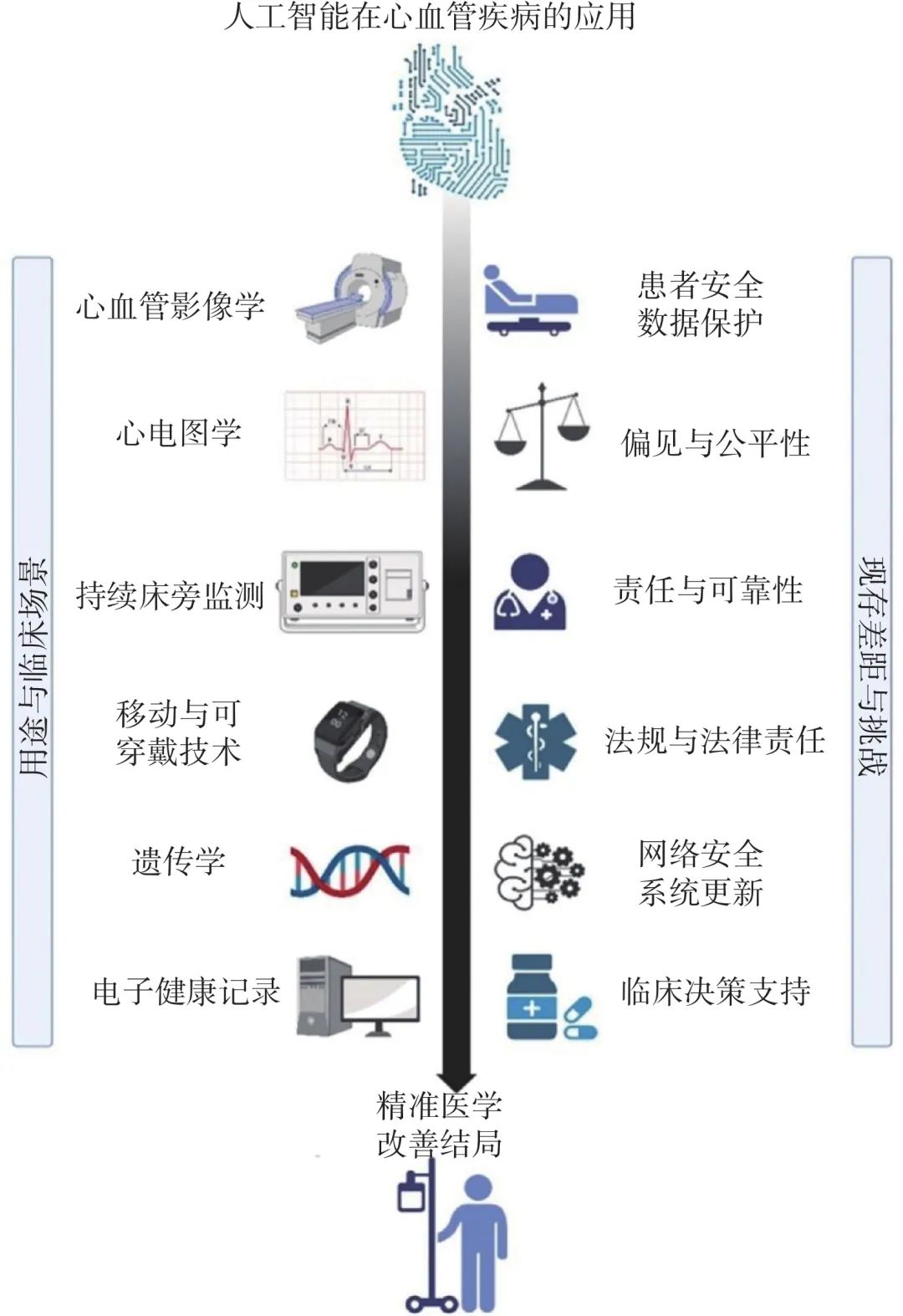
图1 人工智能在心血管疾病的应用[5]
2024年,美国心脏协会(American Heart Association,AHA)发布了《应用人工智能改善心脏病临床结局:AHA科学声明》[5](以下简称“科学声明”)。该科学声明系统总结了AI与机器学习(machine learning,ML)在心血管疾病研究与临床实践中的最新进展,并归纳了当前AI工具的最佳实践模式、现存研究空白及面临的挑战。本文结合笔者团队的相关研究实践,对该科学声明的核心内容进行解读,以期与国内同行分享交流,共同探讨AI在心血管疾病领域的应用前景与发展方向。
1
人工智能/机器学习在心血管疾病诊疗中的应用
1.1 影像
医学影像已成为心血管疾病不可或缺的重要诊断工具。但图像解读需长期训练,影像医师的稀缺加剧了医疗资源分配不均。AI与ML的应用为优化影像分析提供了潜在解决方案,并受到广泛关注[6]。当前,AI/ML算法在医学影像领域的应用涵盖影像检查调度、图像分析、辐射剂量优化、辅助诊断、临床决策支持及预后评估等多个环节[1,7]。
AI/ML在超声心动图领域的应用主要包括心腔自动分割、容积分析及左心室射血分数(ejection fraction,EF)计算,同时可自动评估瓣膜结构、血流梯度、纵向应变及心壁运动异常[8]。
心脏计算机断层成像(computed tomography,CT)已成为AI应用的重要领域,其主要用于冠状动脉(冠脉)斑块及血流的自动量化分析。研究[9]表明,AI可精准测量冠脉斑块(包括钙化及非钙化斑块)及冠脉管腔,与人工测量结果高度一致。此外,AI还可基于心脏CT估算血流储备分数,灵敏度和特异性分别为0.85和0.48,曲线下面积(area under the curve,AUC)为0.76[10]。随着冠脉钙化评分的重要性提升,AI技术可通过低剂量胸部CT自动计算钙化评分,与人工评分相比,AI算法分类准确度超过0.9[11]。
AI/ML技术在心血管磁共振成像(cardiac magnetic resonance,CMR)中的应用日益广泛,已覆盖多个关键分析环节,包括心腔结构及容积的自动识别(与人工标注结果的相关系数r>0.95)、心室和心肌血流量的估算(r≥0.93)以及心肌应变的定量评估(其中周向应变r=0.89,纵向应变r>0.89)[12]。心室晚期钆增强核磁共振成像可用于心源性猝死风险预测,根据纤维化分析识别折返性回路的关键峡部,指导室性心动过速的消融治疗[13]。
AI与ML在结构性心脏病介入治疗中的应用日益广泛。AI/ML可通过快速自动提取冠脉管腔中心线及评估狭窄程度,以辅助冠脉介入治疗。此外,在经导管主动脉瓣置换术、二尖瓣置换术及卵圆孔未闭封堵术中,AI/ML可用于评估二尖瓣环、左室流出道、Valsalva窦及主动脉窦管的解剖参数[8],优化手术规划。
医学影像领域的AI/ML应用面临诸多挑战,数据获取、整理及共享尤为重要(表1[5])。临床影像数据获取困难,多为非结构化或未标注,需结合监督、无监督及半监督学习等方法优化模型性能。
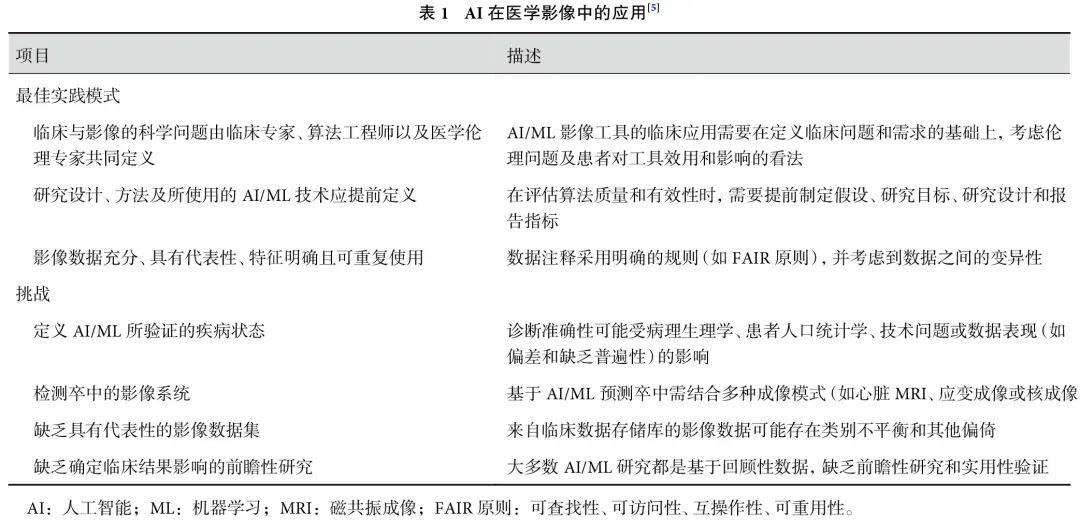
近期发布的AI/ML框架涵盖了对研究问题定义、模型选择、样本量设定及统计方法应用的说明,旨在提升AI研究规范性与可复现性[14]。医学影像数据就绪度量表等工具能进一步促进数据结构化[15]。FAIR原则(可查找性、可访问性、互操作性、可重用性)及NIfTI等标准数据格式的应用,有助于不同研究团队间的数据共享与重复利用[16]。在数据隐私及合规性方面,联邦学习允许研究合作者在不共享原始数据的情况下开发AI/ML工具,保护患者隐私的同时加速算法开发与应用。
1.2 心电图
AI/ML技术在心电图(electrocardiogram,ECG)分析中有重要应用,能够实现自动化解读,提高解析效率,满足日益增长的检查需求。此外,AI/ML能够识别复杂的非线性模式,增强疾病表型分析能力,对心脏电活动异常的早期识别至关重要[17]。
AI/ML技术不仅能够扩展专家的ECG解读能力,还能超越传统人工判读的局限。在隐匿性结构性心脏病的识别中,AI/ML较传统方法可提前1~2年发现疾病[18]。在一项前瞻性研究[19]中,AI-ECG分析在初级保健诊所的应用,使心室功能障碍的首次检出率提高了32%,AUC达0.92(P<0.007)。一项在英国开展的类似研究[20]采用基于听诊器的ECG设备结合AI算法,也证实其优于常规筛查。此外,AI/ML技术在心房颤动(atrial fibrillation,AF)检测中也展现出潜力,其在窦性心律患者中检测隐匿性AF的AUC达0.87,95%置信区间(confidence interval,CI)为0.86~0.88[18]。然而,AI/ML在AF预测和卒中风险评估中的作用仍需进一步研究。
此外,AI/ML技术在ECG表型分析中也展现出其独特价值。研究者[21-22]通过AI/ML分析ECG,成功预测性别和生物学年龄。Ahmad等[22]纳入275056例患者,AI/ML算法在性别预测中的准确率达90.4%(AUC=0.97)。在年龄预测方面,AI/ML算法的估算值与实际年龄的平均偏差为(6.9±5.6)岁。值得注意的是,AI/ML预测年龄较实际年龄高出7岁以上的患者往往合并左心室EF降低、高血压及冠脉疾病等“生物学年龄提前”的相关因素。该研究结果表明,AI/ML技术不仅可辅助传统ECG解读,还可提供个体健康状况相关的生物学信息。
尽管AI/ML在ECG分析中展现出巨大潜力,但其临床应用仍面临诸多挑战(表2[5])。首先,大规模、多样化人群中的临床验证对于算法开发至关重要。其次,自动化偏倚、模型稳健性以及过拟合等问题限制了其在临床实践中的广泛应用。此外,ECG数据的数字化程度有限,高质量、严格标注的开源数据集较为稀缺,制约了AI/ML算法的发展。目前,AUC是评估AI/ML模型性能的主要指标,但针对该类技术的最优评估方法尚未确定,仍需进一步研究。
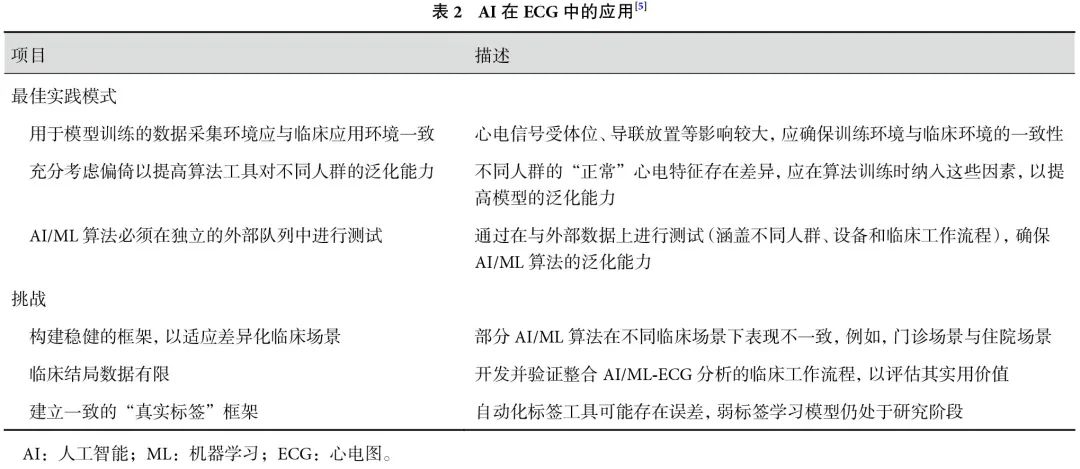
1.3 院内监测
AI/ML技术通过分析连续的院内监测数据流,能够从多种同步采集的信号中提取微妙特征,实现更精准的生理状态评估,提高早期预警系统的准确性,进而改善患者临床结局。
AI/ML显著提升了床旁监护系统的精准度。首先,AI/ML能够降低误报警率,通过卷积神经网络(convolutional neural networks,CNN)分析重症监护病房生命体征数据,有效区分真实警报与误报警,减少“警报疲劳”,提升临床警报系统的有效性[23]。其次,AI/ML模型能够检测细微的生理特征变化,在恶化情况发生前提供预警,延长诊断和治疗的窗口期。一项研究基于极端梯度提升(extreme gradient boosting,XGBoost)模型,利用心率和呼吸频率数据,可在室性心动过速发生前1 h准确预测,敏感度和特异度均超过0.80[24]。结合ECG、非侵入性血压及经皮血氧饱和度等数据,可进一步提升预测性能。
此外,AI/ML在预测院内心律失常发生方面具有应用潜力。基于MIMIC-Ⅲ数据库,研究[25]表明,AI/ML在术后AF的预测上AUC为0.59~0.74,优于传统评分系统。AI/ML基于EHR可预测AF重症患者住院期间的卒中/短暂性缺血发作及大出血事件,AUC分别达0.931和0.93,显示出较高的预测性能[26]。在药物相关心律失常预测中,AI/ML技术能够评估药物诱发心律失常的风险,如deepHerg模型能够预测药物阻断钾通道的能力,C统计量值达0.967,为监测药物相关心律失常提供了重要支持[27]。
AI/ML在围手术期风险评估中的应用优于传统临床评分系统。在瓣膜或冠脉旁路移植手术患者中,CNN分析ECG可预测长期住院患者的死亡率[28]。在术中,AI/ML应用于脑电图可提取谱特征,以评估麻醉深度并优化麻醉剂量调整,从而降低术后谵妄风险[29]。此外,AI/ML分析术中变量,可提前预测低血压、心律失常和低氧血症的发生。
尽管AI/ML在院内监测中展现出巨大潜力,但其临床应用仍面临多重挑战(表3[5])。现有研究[30]表明,AI/ML系统在某些情况下报告的死亡率下降可能更多地源于被监测个体的行为改变(霍桑效应)。其次,AI/ML工具在实际应用中受限于标准化临床报告平台的缺失以及门诊数据中的噪音干扰,有效数据监测时间往往仅占总监测时间的一半。未来研究需从长时间段内提取更具信息量的时变指标,并通过优化试验设计方案,克服这些挑战。

1.4 植入式和可穿戴技术
AI/ML技术通过植入式和可穿戴设备持续监测数据,为疾病进展提供新见解,并优化干预时机,重新定义住院与门诊护理的界限。此外,AI/ML与远程设备的结合能够有效缩小地区间医疗水平差异。
Apple Heart研究[31]和WATCH-AF试验[32]证实了AI/ML结合脉搏波描记设备可应用于AF检测。Hannun等[33]的研究表明,AI/ML分析ECG数据可以识别12种心律类型,并且与专家水平相当,结合智能手机加速度计或陀螺仪数据,AI/ML分析可将AF检测准确率提高至90%以上,并可用于检测室性心动过速和心室颤动。AI/ML技术亦可进行血压估算,该任务的关键参数包括脉搏传播时间和脉搏到达时间,为无袖带血压监测提供新技术路径[34]。此外,AI联合远程设备还能够辅助疾病管理。例如,多中心LINK-HF研究利用AI/ML分析胸部贴片数据可监测心力衰竭(heart failure,HF)加重及预测再住院事件,敏感性达88%,特异性达85%[35]。
笔者认为,AI/ML辅助的远程医疗领域仍需解决的问题包括:识别最适合AI/ML远程监测的患者和疾病类型,并为每种疾病开发并验证有效的护理路径。此外,AI/ML处理移动设备数据可能引发伦理问题—尽管数据所有权归患者所有,但数据隐私性、可操作性和完整性需由所有利益相关方共同维护,然而目前尚未建立针对AI/ML驱动的远程医疗设备的监管框架(表4[5])。

1.5 遗传学
过去10年间,高通量DNA测序的技术突破产生了海量的人类遗传学信息。基于遗传信息,结合个体长期随访的表型与生活方式数据,AI/ML模型得以从遗传和环境等维度全面预测疾病发生风险。
AI/ML技术在全基因组关联研究和多基因风险评分中的应用显著提升了遗传变异与疾病关联的解析能力。如Jo等[36]利用CNN识别与疾病相关的单核苷酸多态性,并构建分类模型,为复杂疾病的遗传风险预测提供了新思路。在多基因风险评分构建时,传统线性模型的解释力有限,而AI/ML技术通过考虑单核苷酸多态性间的相互作用和非线性关系,显著提高了表型变异的解释率。如Elgart等[37]基于多种族基因组数据,结合XGBoost算法,成功提高了9种复杂表型的预测精度。
AI/ML技术在基因功能鉴定和表型驱动的基因分析中也展现出巨大潜力。在基因功能鉴定方面,AI/ML模型通过整合进化保守性分析和变异功能预测,优化了意义不明变异的分类准确性。例如,PrimateAI基于CNN,仅依赖DNA或蛋白质序列,实现了意义不明变异的高精度分类[38]。在表型驱动的基因分析中,AI/ML技术通过表型分析,能够显著提升遗传病的早期筛查能力。例如,DeepGestalt算法基于面部图像在识别单基因遗传综合征方面优于临床专家[39],而基于ECG的深度学习(deep learning,DL)模型在长QT综合征的检测中表现出超越心脏病学家的准确性,并可进一步区分长QT综合征的常见遗传突变[40]。
尽管AI/ML在遗传学领域的应用已取得显著进展,但其作为最终分类工具仍需谨慎对待(表5[5])。AI/ML模型的训练依赖于人类数据,而数据本身可能存在误差和不一致性,可能导致复杂基因变异与疾病的关系在解析中存在偏差。此外,模型的解释性问题也限制了其在临床实践中的广泛应用。

1.6 电子健康记录
与传统随机对照试验仅在单一时间点评估单一治疗方案不同,AI/ML基于EHR数据的分析能够模拟连续决策过程,涵盖所有接受或未接受干预的患者,以探索临床场景下的干预效果异质性。尽管已有多个基于EHR的AI/ML应用被报道,但大多数仍局限于其开发队列,尚未推广至广泛患者群体。
AI/ML技术在疾病预测领域已展现出显著优势。在重症监护病房死亡率预测中,算法模型通过分析17个静态变量,在测试人群中实现了AUC为0.94[95%CI(0.90,0.98)]的预测性能[41]。AI/ML模型在心血管疾病预测中也表现出色,Zhao等[42]开发的AI/ML工具在109 490名个体中对10年内心血管事件的预测性能优于美国心脏病学会/AHA风险方程。在特定心血管疾病的预测中,AI/ML模型同样优于传统方法。Ye等[43]基于XGBoost算法开发的模型对680 810例前瞻性研究对象1年内发生原发性高血压的预测AUC达0.870。Guan等[44]利用EHR数据对缺血性卒中患者的预测准确率为92.2%,AUC为0.911[95%CI(87.5,93.9)]。此外,AI/ML技术通过整合多模态数据实现心血管疾病的精准分型。例如,在HF分类中,传统方法主要基于EF,而AI/ML模型能够识别具有不良预后风险的HF患者,预测心脏骤停高风险个体,以及筛选可能对消融治疗产生良好反应的AF患者。
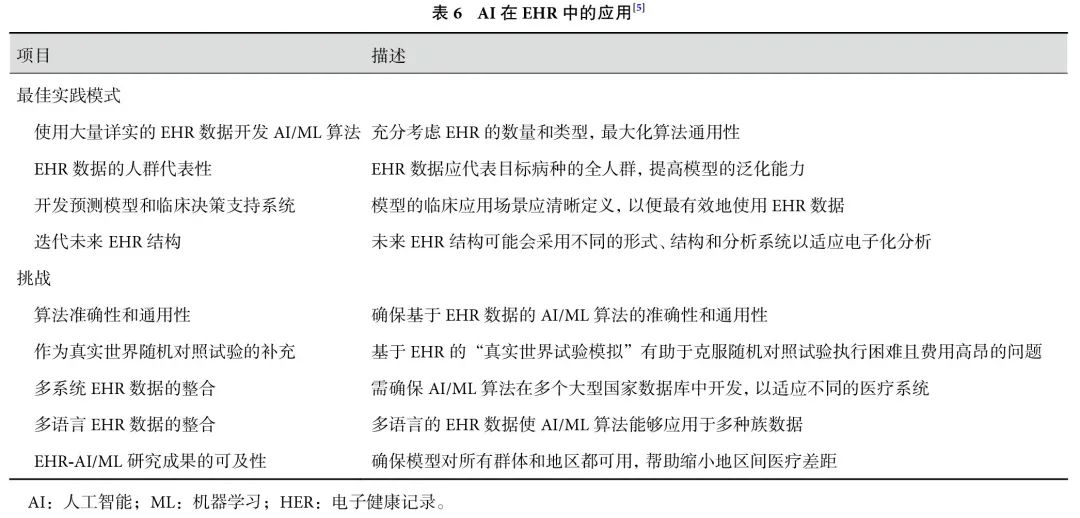
尽管AI/ML技术在EHR分析中展现出巨大潜力,但其应用仍面临诸多挑战(表6[5])。首先,不同中心EHR数据来源于不同的信息系统,可能导致数据的差异性。其次,EHR分析可能引入多种偏倚,例如测量频率与疾病严重程度的相关性,以及入院标准和治疗方案的个体化差异。再者,EHR数据通常缺乏社会因素及其他潜在混杂变量,且不同机构和地区间的差异性随时间变化,使研究结果难以推广。生成式AI/ML的发展为临床医师和研究人员提供了新的机遇。
2 人工智能/机器学习在心血管医学中成功实施的框架
2.1 基于人工智能/机器学习精准医学的实施科学
实施科学专注于研究如何将科学研究成果或循证实践有效运用至日常医疗卫生实践中,以提高常规卫生服务质量[45]。AI/ML的实施科学对整合个人和公共数据,满足心血管医学的临床需求至关重要(表7[5])。

科学声明强调,AI/ML的角色定位应是辅助临床决策,而非取代基于循证医学的临床判断。为实现AI/ML在心血管领域的广泛应用,需通过直观且可解释的人机界面将AI/ML分析结果呈现给临床医师,以增强信任并整合到现有工作流程中。其次,AI/ML算法需经药械监督管理部门认证,明确适用人群和临床场景,随着研究扩展至新患者群体,认证范围需相应更新。再者,AI/ML系统需定期更新和重新评估,避免因患者特征或临床背景变化导致性能下降。笔者认为,未来AI在心血管医学中的应用程度将取决于能否证明其可改善患者临床结局,目前尚缺乏设计良好的随机对照试验证明AI/ML在改善患者预后方面优于现有治疗标准。
2.2 数据处理与伦理
数据处理细节(如重新编码、导出、排除或变换)可能显著影响模型的解释性和准确性。目前,已有指南[46]旨在提高AI/ML衍生决策支持系统设计的严谨性和可重复性。AI/ML数据库的数据贡献者应得到尊重,大多贡献者不希望其数据在未经通知或同意的情况下被出售给第三方用于商业目的。因此,数据使用的透明度和知情同意至关重要。
2.3 偏倚与医疗公平
AI模型在不同亚群体中的表现差异可能源于社会偏倚和统计偏倚。社会偏倚由系统性歧视导致,表现为边缘化群体在心血管健康结局上的不均衡状态,同时这些群体的数据质量也存在问题。统计偏倚则源于训练数据中非代表性的样本。因此,AI模型可能在整体上表现出较强的性能,但在代表性不足的群体中表现不佳,而这些群体往往面临更严重的健康问题。在医疗AI/ML算法开发中,公平性应作为明确的核心目标。为实现医疗公平的目标,需从数据集的选择、模型构建以及研究团队的组建等多方面采取措施:必须纳入具有人群代表性的数据集,将来自代表性不足群体的个体纳入AI/ML模型构建过程,并组建更加多元化的研究团队。
2.4 法规与政府监管
法律在AI/ML领域的应用主要分为两类:通过监管措施减轻AI/ML潜在危害,或通过医疗过失判罚系统补救已由AI/ML导致的损害。美国食品药品监督管理局将AI/ML作为医疗器械进行监管,并重申了其对改善AI/ML算法的承诺:旨在减轻偏见并提高其稳健性[47]。目前,美国食品药品监督管理局心血管医疗器械清单中已批准50项AI/ML技术,并批准了5项创新请求。
AI/ML治理架构需与开发者、临床医师和研究人员合作,持续评估算法的安全性和有效性。企业应向药械监督部门提交申请,以允许算法上市。获批后,需进行上市后安全监测,类似于药物开发的Ⅳ期评估。在此持续阶段,若算法使用导致潜在不良事件,其责任由AI/ML算法开发者负责调查并报告。临床医师在面对算法提供错误决策和潜在有害结果时的职业责任划分,应与其他医疗产品一致,按“按照标签使用”医疗器械的责任进行划分。
2.5 系统更新与网络安全
决策支持系统需要定期更新,以减小数据质量、人群特征和临床实践随时间变化对其可靠性、有效性和临床实用性的影响。此外,随着对疾病科学理解的进展或AI/ML算法使用地区人口结构的变化,可能需要更新结果定义以重新训练模型。部分AI/ML算法可设计为持续训练,以优化模型并提升性能。数据隐私问题仍然存在,开发者需设置适当的防火墙和其他关键网络安全措施,并定期更新,以确保数据安全。数据相关方可以设定一个可接受的风险阈值,低于该阈值时允许数据共享,以促进全球医学知识系统的信息互通。
3 国内心血管领域人工智能/机器学习研究进展
国内研究团队在AI辅助心血管疾病的风险预测、诊断、治疗和临床研究方面的探索性工作取得了诸多成果,推动了AI和数字健康工具在心血管领域的深度融合。
在AI辅助影像诊断方面,国内研究取得了显著成果。南京大学鼓楼医院团队[48]基于DL实现对CT血管造影(computed tomography angiography,CTA)结果的自动化钙化评估,为心血管疾病的早期筛查提供了重要工具。阜外医院团队的研究[49]证明了端到端基于视频的DL模型可以从CMR数据中检测心脏异常并进一步分类不同的心血管疾病,展现了该技术在心脏影像分析中的应用潜力。此外,广东省人民医院的研究团队[50]基于CT数据开发了与专家水平相当的AI诊断系统,成功识别了17种先天性心脏病,进一步验证了DL在辅助复杂病例诊断方面的可靠性和准确性。
国内研究团队在探索多模态预测心血管疾病风险方面进行了诸多创新性尝试。来自香港中文大学[51]和北京大学[52]的研究团队基于DL的自动化眼底图片视网膜血管测量系统能够提供优于专家的测量结果,该测量结果可预测心血管疾病的未来发生风险。来自阜外医院的另一研究团队[53]基于CNN,利用5796例患者的面部特征构建了冠心病诊断模型,并在1013例接受冠脉造影或CTA检查的患者中进行了验证。研究结果表明,该基于面部照片的AI检测方法在准确度上显著优于Diamond-Forrester模型及冠心病联盟临床评分。与此同时,清华大学研究团队[54]采用红外热成像技术,在冠脉疾病确诊检查前收集患者面部热成像数据,并借助DL方法构建预测模型。该研究进一步对比了AI赋能的红外热成像方法与国际指南推荐的验前概率模型,发现AI模型在冠心病的预测性能上具有更优表现。
除了疾病诊断,AI算法工具也在慢性病管理中展现了巨大的应用潜力。解放军总医院开展的研究[55]表明,采用“互联网+”远程互动管理策略能够显著改善高血压患者的血压控制效果。研究显示,通过远程管理,患者的血压达到目标值的时间显著缩短,体现AI技术在临床研究中的作用。
近年来,国内以DeepSeek为代表的大语言模型快速涌现和迭代,面向心血管疾病的领域垂直大模型逐渐出现。上海交通大学研究团队[56]开发了基于ECG的AI诊断大模型—KED模型,该模型以来自近16万例患者的80万份ECG作为训练集,并在多地区人群的ECG数据上进行了测试。结果显示,该大语言模型具有与ECG专家相当的诊断精度。近期,北京大学的一项研究[57]提出了MedFound-DX-PA疾病辅助诊断通用大模型,其在心脏亚专科常见病的诊断上达到近75%的准确率。
4 总结与展望
在精准医学时代,临床医师、数据科学家、患者权益团体、医疗机构以及政策制定者需要共同制定AI/ML工具在数字健康领域的发展与应用指南。目前,AI/ML工具已展现出巨大潜力,可用于改善疾病筛查、分析个体患者的健康特征,并为复杂疾病开发精准治疗方案。当下,迫切需要制定AI/ML工具的实施科学,以创建高效、低成本的精准医疗工作流程,解决未满足的临床需求。这些工作流程需通过试验验证其有效性,并确保消除偏见,最大化研究结果的普适性,避免加剧医疗健康不平等。
结合笔者所在团队的实践体会,未来心血管领域AI/ML工具的发展趋势主要概括为以下几个方面。
(1)多模态融合与精准医学。随着计算资源的不断拓展,AI模型能够接收多样化形式的输入数据。一些突破传统危险因素、非线性相关的信息源作为输入数据用于训练模型。未来,整合个体遗传学信息、蛋白组学、代谢组学、社会因素、生活方式信息等多维度数据的AI模型有望出现,其将服务于疾病筛查、诊断、治疗以及预后评估的全流程,实现AI时代精准医学的诊疗模式。
(2)提高模型可解释性。随着AI/ML技术在医疗领域的深入应用,如何提高AI模型的透明度和可解释性成为了一个重要课题。特别是在医疗决策中,医师和患者需要了解AI模型的决策依据,以增加其信任度并确保治疗的合理性。AI的“黑箱效应”使得其决策过程难以理解,这也成为AI在医学应用中遇到的主要挑战之一。实现可解释性的方法包括通过可视化技术、局部解释模型以及基于规则的模型(如决策树模型)揭示AI模型如何得出诊断结论。
(3)弱监督模型或自学习算法。传统的监督学习模型依赖大量的标注数据进行训练,但在医学领域,获取大规模高质量标注数据往往面临挑战。弱监督学习和自学习算法能够有效应对医学数据标注不足的挑战,推动数据驱动的医学研究和应用。通过自动化学习和调整,这些模型能够在不依赖大量标注数据的情况下,不断提升自身的准确性和可用性,为临床提供强有力的辅助决策支持。
(4)基于AI工具新型诊疗模式的前瞻性探索。AI工具的进步可能催生一些新的医疗模式,例如基于AI的个性化治疗平台,能够实时监测患者的健康状况,并根据其生理数据变化动态调整治疗方案。通过这种“AI驱动的闭环治疗”,可以实现对患者健康状态的持续跟踪和优化。但此类诊疗模式还需在真实世界中设计前瞻性研究以验证其有效性和安全性。
(5)AI与可穿戴设备嵌合的远程医疗模式。AI与可穿戴设备结合的远程医疗模式将改变传统治疗方式,使疾病管理更加灵活、即时。这种模式不仅能为患者提供更好的健康监测,还能在突发状况下实现快速反应,为慢性病患者提供更稳定的健康保障。
(6)电子健康数据的标准化与共享。AI的广泛应用需要通过标准化的数据格式与共享平台来实现数据的高效流动和利用。统一的标准可使不同医疗机构之间的数据兼容,AI模型能够更好地训练和优化,提升诊断、预测和治疗的效果。诸如CardiaCare的多中心临床科研创新平台[58],为心血管领域数字信息标准化及数据库共享提供了重要推动,也为基于多中心数据开发稳健AI工具创造了条件。
(7)AI辅助手术机器人。在心血管手术中,AI辅助手术机器人有望根据患者的生理特征提供实时数据支持,在关键步骤中提供辅助决策,并且准确预测围手术期并发症和死亡率,优化患者选择、临床试验设计及知情同意流程,从而提升手术安全性和预后。此外,AI还能够通过增强现实技术,提供可视化的实时导航,帮助外科医师进行精准操作。
利益冲突:无。
作者贡献:陈锦华、张恒撰写初稿;郑哲审阅并修改。


