【爱儿小醉】抗纤溶药物和辅助止血药物:儿科体外膜肺氧合抗凝协作共识会议
时间:2025-08-26 12:11:01 热度:37.1℃ 作者:网络

引言
小儿体外膜肺氧合(ECMO)作为一种生命支持手段,广泛应用于新生儿和儿童的重症治疗中,尤其在呼吸衰竭或心脏衰竭等危急状态下,为患者提供至关重要的支持。然而,ECMO治疗伴随的并发症,如出血和血栓形成,依然是临床面临的重大挑战。抗凝治疗和止血管理在ECMO治疗中的角色显得尤为重要,但在儿科患者中的使用策略和具体方法仍存在许多争议和不确定性。
抗纤溶药物(如ε-氨基己酸[EACA]和氨甲环酸)以及辅助止血药物(如重组活化凝血因子Ⅶ [rFVIIa]和局部止血剂[THA])常用于体外膜肺氧合(ECMO)过程中,以降低出血风险并预防血栓并发症。然而,这些药物在儿科患者中的使用效果和安全性尚无统一共识。为填补这一研究空白,儿科体外膜肺氧合(ECMO)抗凝协作组(PEACE)联合多个国际专家,基于系统评价,采用改良德尔菲法开展了抗纤溶和辅助止血药物使用的共识制定工作。本文将介绍最近发表于《Pediatric Critical Care Medicine》杂志的文章,题为“Antifibrinolytic and Adjunct Hemostatic Agents: The Pediatric Extracorporeal Membrane Oxygenation Anticoagulation Collaborative Consensus Conference”,该文章总结了该领域的最新共识。
本共识旨在通过文献系统回顾和专家意见相结合,评估现有药物治疗策略的有效性和安全性,并为儿科ECMO支持的新生儿和儿童患者制定合理的抗凝与止血管理方案。通过对1988年1月至2021年5月期间的文献进行全面检索和分析,结合专家的临床经验,我们旨在提出基于证据的推荐意见,并在证据不足的情况下,通过专家共识达成指导声明,推动儿科ECMO治疗领域的进一步发展。
本研究将对当前抗纤溶药物、重组活化因子Ⅶ及局部止血药物的使用情况进行综合评估,并就如何在临床实践中合理应用这些药物提出指导建议,为提高儿科患者ECMO治疗的安全性和效果提供理论依据。
方法
临床相关出血的详细方法和定义在《PEACE执行摘要》中有描述。简而言之,我们利用医学主题词和文本词相结合的方式,于1988年1月至2020年5月期间在PubMed、EMBASE和Cochrane图书馆(CENTRAL)数据库中进行了结构化文献检索,并于2021年5月进行了更新,以研究接受体外膜肺氧合(ECMO)支持的儿科患者(人群),对比抗纤溶药物(氨甲环酸或氨基己酸)、重组人凝血因子Ⅶa、血栓弹力图指导的治疗(THAs)或止血治疗方案或止血药物组合(干预措施)与标准/保守措施或其他止血药物(对照)对结局的影响(结局)(补充方法,http://links.lww.com/PCC/C491)。两名作者独立审阅引文,若有任何分歧则由第三位独立审阅者解决。使用标准化数据提取表构建证据表。根据具体情况,采用预后研究质量(QUIPS)工具或修订后的Cochrane随机试验偏倚风险评估工具来评估偏倚风险,并使用推荐分级的评估、制定与评价(GRADE)系统对证据进行评价。一个由48名专家组成的小组在两年多的时间里召开会议,制定基于证据的推荐意见,在缺乏证据时,则制定基于专家共识的声明。使用证据到决策框架对支持性文献进行审查并制定声明,强调小组对每项拟议声明的风险与获益的评估,以及通过对专家小组成员进行网络调查而创建的患者结局优先列表。采用基于网络的改良德尔菲法,通过研发/加州大学适宜性方法达成共识。共识定义为同意率超过80%。其他未纳入结构化文献检索的参考文献,在理由陈述中列出以提供背景信息,但不用于得出推荐意见或共识声明。
结果
结构化文献检索确定了3550条引文,其中3424条根据摘要被排除。根据全文审查,又排除了115篇参考文献,最终留下11篇参考文献用于提出推荐意见和制定共识声明(图1)。纳入的参考文献详见补充表1(http://links.lww.com/PCC/C491)。偏倚风险评估总结见补充图1(http://links.lww.com/PCC/C491)。制定了1条弱推荐意见和3条共识声明,并达成一致(>80%)。
全身抗纤溶及止血药物
共识声明
6.1 对于正在出血或预计有高出血风险的体外膜肺氧合(ECMO)患者,作为多模式血液管理策略的一部分,可考虑使用赖氨酸类似物抗纤溶药物(ε-氨基己酸、氨甲环酸)来减少出血。共识小组专业意见,一致性较弱,一致性93%(n=46),中位数8(四分位数间距7 - 9)。
证据总结:四项研究对氨甲环酸(EACA)进行了调查。将因 “高出血风险” 接受预防性氨甲环酸治疗的新生儿回顾性队列与历史队列以及未接受氨甲环酸治疗的 “低风险” 新生儿进行了比较。“高出血风险” 因素包括外科手术、缺氧、酸中毒、凝血病、早产或颅内出血(ICH)。氨甲环酸给药方案为插管时静脉推注100毫克/千克,随后以30毫克/千克/小时的速度输注,直至拔管。接受该方案治疗的新生儿出血较少,所需血液制品也较少,其中先天性膈疝(CDH)和先天性心脏病患者的差异最为明显。接受氨甲环酸治疗的患者未出现颅内出血(ICH)。
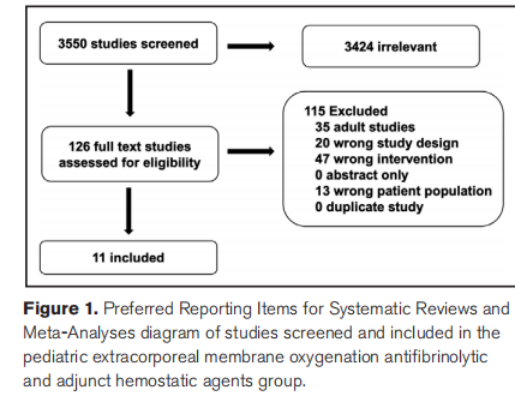
图1. 系统评价和荟萃分析的首选报告项目。儿科体外膜肺氧合抗纤维蛋白溶解剂及辅助止血剂研究的筛选及纳入研究图示。
在对照组中,颅内出血发生率为12%,而使用氨甲环酸(EACA)后血栓形成并发症的发生率虽有所增加,但差异无统计学意义。随后一项针对接受体外膜肺氧合(ECMO)的新生儿使用预防性氨甲环酸(EACA)的随机对照试验采用了上述方案。输血需求、出血和血栓形成并发症情况相似;然而,使用氨甲环酸(EACA)后颅内出血发生率有升高趋势。一项针对因“高出血风险”而接受预防性氨甲环酸(EACA)治疗的体外膜肺氧合(ECMO)患者的回顾性研究,将结果与“低风险”机构对照组和体外生命支持组织(ELSO)的数据进行了比较。与体外生命支持组织(ELSO)的数据相比,使用氨甲环酸(EACA)的患者需要更频繁地更换回路,手术部位出血较少,颅内出血、血栓形成并发症和死亡率相似。与机构对照组相比,输血需求和患者相关血栓形成情况相似;然而,观察到回路更换频率更高。一项针对儿科体外膜肺氧合(ECMO)的回顾性研究比较了标准治疗、出血及高风险方案(使用和不使用氨甲环酸(EACA));各治疗组之间回路更换频率相似。
一项历史对照研究对接受体外膜肺氧合(ECMO)的先天性膈疝(CDH)新生儿使用预防性氨甲环酸的情况进行了研究。给药剂量和时机并不一致;然而,使用氨甲环酸的患儿出血和输血情况较少,血栓并发症发生率相近。
较小规模的系列研究报告了儿科围手术期体外膜肺氧合(ECMO)中使用抗纤溶药物的情况,包括心脏手术后、肺活检以及先天性膈疝(CDH)手术。有关儿科ECMO围手术期管理,详见PEACE关于围手术期儿科ECMO管理的共识建议。在一项针对先天性膈疝(CDH)和体外膜肺氧合(ECMO)的历史对照研究中,使用氨甲环酸(EACA)与围手术期失血量减少、输血需求降低、手术再次探查减少相关,且生存率提高,血栓并发症或颅内出血(ICH)无统计学意义的增加。也有支持性数据表明抗纤溶药物可用于成人ECMO患者的出血治疗或预防。与我们的声明一致,基于类似数据,胸外科协会和心血管麻醉医师协会血液保护特别工作组主张考虑使用抗纤溶治疗以减少ECMO患者的出血并发症(IIa类推荐)。
获益与危害的平衡:高质量数据的缺乏、研究的异质性、不一致的研究结果、最佳剂量的安全性数据有限以及潜在的并发症,产生了关于赖氨酸类似物抗纤溶药物的一份经过充分讨论的共识声明。这一共识观点涵盖了氨甲环酸(EACA)和氨甲苯酸,这两种药物之间的证据相当一致,并且在指南声明中有同时使用这两种药物的先例。
其他注意事项:异质性:纳入及支持性数据在人群、抗纤溶适应症(如出血或预防)以及高风险定义方面存在差异。最佳方案仍不明确,文献报道的剂量、间隔时间和疗程各不相同。尽管一项关于体外膜肺氧合(ECMO)中使用6 - 氨基己酸(EACA)的体外研究发现,该药物在循环系统中无明显潴留,但即使在研究较多的心脏手术人群中,给药问题依然存在。在所有研究中,报道的疗效并不一致,且对血栓事件、安全性和药代动力学的描述有限。在心脏手术中,推荐术中预防性使用抗纤溶药物;然而,有报道称使用氨甲环酸会使癫痫发作风险增加7倍。需要进一步研究抗纤溶药物在儿科体外膜肺氧合中的应用,从而为循证推荐提供依据。
年龄:为该建议提供依据的纳入数据主要来自新生儿,不过预计研究结果适用于各年龄段儿童。
受体:赖氨酸类似物抗纤溶药物(6-氨基己酸、氨甲环酸)可逆地与纤溶酶原结合,阻止其转化为纤溶酶,纤溶酶是一种可降解纤维蛋白的丝氨酸蛋白酶。抑肽酶是一种非特异性丝氨酸蛋白酶抑制剂,传统上也被纳入,在抗纤溶类药物中,[该药物]未被纳入推荐范围。随着《使用抗纤溶药物进行血液保护试验》的发表,抑肽酶不再常规用于治疗出血。
给药途径:没有数据符合替代给药途径的纳入标准。有证据表明,局部使用抗纤溶药物(如浸湿的纱布),与静脉注射剂量无关,可能会减少心脏手术部位或口腔出血。已有文献报道使用不同剂量的吸入或支气管镜下应用氨甲环酸治疗危及生命的肺出血,疗效各异。
共识声明:
6.2 对于体外膜肺氧合(ECMO)患者 - 由于存在血栓并发症风险,我们不建议使用VIIa因子(重组VIIa因子,rFVIIa),除非出现危及生命的出血,且采用多模式血液管理和复苏措施处理导致出血的因素后出血仍难以控制。专家共识小组达成高度一致,96% 的共识 (n=46),中位数8(四分位间距7 - 9)。
证据总结:一项回顾性病例系列研究评估了重组活化凝血因子VII(rFVIIa)在接受体外膜肺氧合(ECMO)治疗且有出血症状的儿科患者中的应用,将接受rFVIIa治疗的患者与历史对照患者进行比较。使用rFVIIa后,出血和输血需求显著减少,且两组在血栓栓塞并发症、体外循环故障和死亡率方面的发生率相近。其他数据来自三项针对心脏外科手术患者的观察性研究,其中包括接受ECMO治疗的亚组患者。与对照患者相比,接受rFVIIa治疗的新生儿发生临床显著血栓并发症的情况更多。在接受ECMO治疗且有出血症状的儿童中,与仅使用血液制品相比,接受rFVIIa治疗可减少出血量和血液制品的使用;然而,25%的患者发生了血栓事件,其中包括两名出现与患者及体外循环相关严重并发症的ECMO患者。另一项针对接受rFVIIa治疗的ECMO患儿登记册回顾报告显示,尽管剂量存在差异,但治疗有效率为82%,且输血显著减少,血栓栓塞事件发生率为19%。
小型儿科体外膜肺氧合(ECMO)病例系列研究以及儿科心脏外科手术出血相关数据(其中报告将重组人凝血因子VIIa作为挽救疗法控制难治性出血)为我们的声明提供了参考;然而,报告中使用剂量、使用频率各不相同,疗效也不一致,不良事件发生率也有差异。支持有关于成人体外膜肺氧合(ECMO)的数据,且与我们的建议相符。胸外科医师协会和心血管麻醉医师协会血液保护特别小组指出,对于接受ECMO治疗的心脏手术患者,重组人凝血因子Ⅶa(rFVIIa)疗法可能有助于控制危及生命的出血,并建议权衡潜在益处与严重急性血栓并发症的相关报道(IIb级)。在危及生命的出血情况下,尽管采取了手术和纠正凝血功能障碍的措施,rFVIIa仍控制了接受ECMO治疗的成人患者的出血;然而,有患者及回路相关血栓并发症的报道。
获益与危害的平衡:目前尚无确切证据支持在儿童体外膜肺氧合(ECMO)中常规使用重组活化Ⅶ因子(rFVIIa,诺其,丹麦诺和诺德公司,哥本哈根,丹麦)。尽管rFVIIa可能减少出血,但由于样本量较小,且担心会发生包括致命性和急性灾难性事件在内的血栓形成,其总体安全性和临床实用性仍不明确。
其他注意事项:儿科应用及剂量。在体外膜肺氧合(ECMO)中,使用重组活化凝血因子Ⅶ(rFVIIa)治疗危及生命或难以控制的儿科出血属于超说明书用药。重组活化凝血因子Ⅶ是一种维生素K依赖的基因工程糖蛋白,可激活因子Ⅸ和因子Ⅹ,促进凝血酶生成,促使血小板形成纤维蛋白凝块。最佳剂量仍不明确(范围为24 - 174微克/千克,最常报道的为60 - 90微克/千克),给药频率为每1 - 4小时一次,总剂量为1 - 23剂。
其他促成因素:成人研究支持在使用重组VIIa因子之前纠正以下指标:凝血酶原时间大于50%,活化部分凝血活酶时间比值小于正常的2倍,血小板大于50,000/毫升,纤维蛋白原大于1克/升,体温大于36°C,血钙大于2.2毫摩尔/升,血细胞比容大于24%。
给药途径:对于吸入氨甲环酸治疗无效的咯血,吸入重组人凝血因子VIIa已在一项有限的病例系列研究中进行了评估,在获得安全性数据之前,应将其作为威胁生命的顽固性出血的辅助治疗手段。
局部止血剂
推荐意见
6.3 在体外膜肺氧合(ECMO)中,考虑预防性应用非牛源性局部止血剂作为多模式血液管理策略的一部分,在插管时使用,以减少插管部位出血。弱推荐,低质量儿科证据,83% 的一致性 (n=46) 中位数 8(四分位距 7 - 9)。
共识声明:
6.4 在体外膜肺氧合(ECMO)期间,作为包括手术止血在内的多模式血液管理策略的一部分,对于插管部位活动性出血,考虑应用非牛源性局部止血剂是合理的。专家共识小组意见,一致性较弱,同意率83%,(n=46),中位数8(四分位数间距7 - 9)。
证据总结:一项单中心前瞻性随机对照试验,对患有呼吸衰竭的新生儿,在外周体外膜肺氧合(ECMO)插管部位,预防性使用纤维蛋白密封剂(由人外用纤维蛋白复合物和人凝血酶组成)与单独使用标准烧灼法控制止血进行了比较。使用纤维蛋白密封剂在插管部位的止血效果更好(42%对18%),出血量和出血持续时间更少,尽管未观察到输血需求的减少,且出现了两起与产品相关的不良事件(部位感染)。在一组接受体外膜肺氧合(ECMO)的新生儿病例中,这些新生儿因不明原因的大量出血而接受了外科探查,使用纤维蛋白胶(由人源性纤维蛋白原浓缩物和牛凝血酶组成)成功止血。
尽管儿科体外膜肺氧合(ECMO)方面的证据有限,但有大量数据回顾了成人ECMO和心脏手术中使用止血辅助剂(THAs)来止血或预防出血的情况。一项针对接受ECMO支持的出血成人的回顾性分析发现,使用THAs的成功率有限;然而,病例报告描述了基于壳聚糖的产品取得了成功,但不太可能出现进一步有力的参考数据。与我们的观点一致,胸外科医师协会(STS)和国际止血专家小组推测,失控性出血具有重大的临床和经济影响,尽管使用THAs存在潜在风险,但仍可能带来重要益处,因此,作为多模式血液管理方案的一部分,可考虑使用这些药物进行局部止血(IIb类推荐)。
获益与危害的平衡:关于全髋关节置换术(THAs)的这些陈述,其依据是缺乏高质量数据,只能从其他人群的数据进行推断。
由于使用非牛源性凝血酶原激活剂(THAs)在降低出血风险方面具有潜在益处,且相关风险极小,因此建议使用。THAs的潜在风险包括免疫反应、抗体产生以及病毒感染传播,尽管使用非牛源性制剂可将这些风险降至最低。在儿童群体中,有12例报告称,因局部使用牛凝血酶导致抗体交叉反应,引发免疫介导的凝血障碍,并伴有危及生命的出血情况。在成人中,围手术期反复接触局部牛凝血酶会增加抗体滴度;然而,并未发现其与不良事件存在关联。人源性凝血酶在减少出血方面可能与牛凝血酶同样有效,且产生抗体的风险更低,这也为我们建议在有条件的情况下使用非牛源性THAs提供了依据。尽管经过严格的清除步骤,血浆源性产品仍存在潜在的病毒传播风险。合成密封剂和机械制剂的不良事件风险较低。
其他循证决策考虑因素:年龄。为这份共识声明提供信息的纳入数据来自新生儿;然而,预计研究结果适用于各年龄段儿童。
类型:纳入文献描述了基于纤维蛋白的密封剂(非牛随机对照试验和牛病例系列),这是一种生物相容性好、可生物降解、有效的组织粘合剂,由纯化的、病毒灭活的人纤维蛋白原、人凝血酶组成,偶尔还添加病毒灭活的人凝血因子 XIII。根据凝血剂成分,组织粘合剂大致分为活性或非活性,并根据作用机制进行分类(通过肿胀产生的压力为血凝块形成提供支架,与形成气密密封以形成纤维蛋白凝块)。市面上有多种具有不同优势的产品可供选择,尽管在心脏手术中广泛使用,但没有数据支持使用特定的产品。
路线:我们的人群中没有相关数据来提供关于黏膜表面的 THA(组织因子途径抑制剂)或局部抗纤维蛋白溶解剂的使用建议。
结论
尽管对描述接受抗纤溶药物(氨甲环酸或氨基己酸)、重组人凝血因子VIIa和血栓弹力图指导下的血液制品治疗的接受体外膜肺氧合支持的儿科患者预后的文献进行了系统回顾,但证据表明支持性建议稀少且无定论。尽管专家小组就所有问题达成了共识,但证据的强度仅能证实基于专家意见的共识声明或微弱的建议。尽管在适应症、剂量、给药途径和持续时间方面存在普遍的知识空白,且风险 - 收益平衡尚不明确,但在危及生命的出血情况下,仍经常使用抗纤溶药物或止血浓缩剂。要确定有效且安全的使用策略,仍有大量工作要做。
爱儿小醉 点评
本文对抗纤溶药物(如氨甲环酸和氨基己酸)、重组活化凝血因子VIIa(rFVIIa)和局部止血剂(THAs)在儿科体外膜肺氧合(ECMO)治疗中的应用进行了系统回顾,并提出了专家共识建议。氨甲环酸和氨基己酸作为抗纤溶药物,主要通过抑制纤溶酶原转化为纤溶酶,从而减少出血。这些药物能够有效减少术中出血和输血需求,尤其在ECMO治疗过程中具有潜力。氨甲环酸(EACA)和氨基己酸(EACA)在成人ECMO中的使用已有一定基础,但在儿科患者中的效果和安全性仍不明确,最佳剂量、给药途径和使用时机尚需进一步研究。
尽管如此,目前的证据相对薄弱,推荐意见的强度较低。对于rFVIIa的使用,虽然在危及生命的出血中有所支持,但其引发血栓的风险仍需谨慎评估。局部止血剂在新生儿中的初步应用显示了效果,但长期的安全性仍然缺乏足够的研究支持。总体来说,本文为儿科ECMO中的抗凝与止血管理提供了框架,但要确定有效且安全的使用策略,仍需要更多高质量的研究。
原始文献
Moynihan KM, Ryerson LM, Le J, et al. Antifibrinolytic and Adjunct Hemostatic Agents: The Pediatric Extracorporeal Membrane Oxygenation Anticoagulation CollaborativE Consensus Conference. Pediatr Crit Care Med. 2024;25(7 Suppl 1):e44-e52.


