Nat Med:渐冻症研究范式转变!基于血浆蛋白质组的ALS诊断模型AUC达98.3%,可提前10年预估发病
时间:2025-08-27 12:10:53 热度:37.1℃ 作者:网络
肌萎缩侧索硬化症(ALS)俗称“渐冻症”,是一种罕见的致命性神经系统疾病,主要影响大脑和脊髓中的运动神经元,导致患者肌肉无力、萎缩和瘫痪,最终危及生命。ALS的早期症状一般不明显,容易被忽视。目前,ALS的诊断依赖于临床症状和神经学评估,患者通常在延迟6-18个月后才被确诊,阻碍了患者的预后。虽然神经生理学研究和基因检测可以作为临床决策的辅助工具,但目前还没有明确的ALS诊断检测。此外,已有运动神经元功能分析方法很难将ALS与其他神经系统疾病区分开来,因为该疾病的临床表现各不相同。因此,ALS亟需能够区分ALS和相似疾病的生物标志物,并预测该疾病何时会显现。
近日,美国国家卫生研究院(NIH)国家老龄化研究所(NIA)研究团队通过生成和分析大型ALS病例对照队列中约3000种血浆蛋白的数据,解决了这一关键的知识空白。通过对比ALS患者与对照组的血浆样本,研究发现33种蛋白质存在显著差异表达,并在独立队列中进行了验证。基于这些蛋白质和临床特征,研究团队利用机器学习创建了一个ALS诊断模型,该模型具有高准确率,AUC达98.3%,可以有效地将ALS病例与健康个体和其他神经系统疾病区分开来。此外,通过分析ALS症状出现前患者的血浆样本,研究还利用该模型预估了发展为ALS的无症状个体何时会出现症状,发现该疾病进程在症状出现前最高10年就可以检测到。该研究结果意味着基于血液的生物标志物可能为ALS诊断和预后提供新的可靠工具,为推进相关致命性神经退行性疾病的生物标志物研究提供了重要资源。

主要研究内容
研究团队利用Olink Explore 3072分析了参与者血浆样本的2,886种蛋白质。研究队列包括231名ALS患者和384名对照(214名健康个体和170名其他神经系统疾病患者),其80%的样本被随机指定为发现队列(183例ALS病例、172例健康对照和137例其他神经系统疾病),其余样本为验证队列。
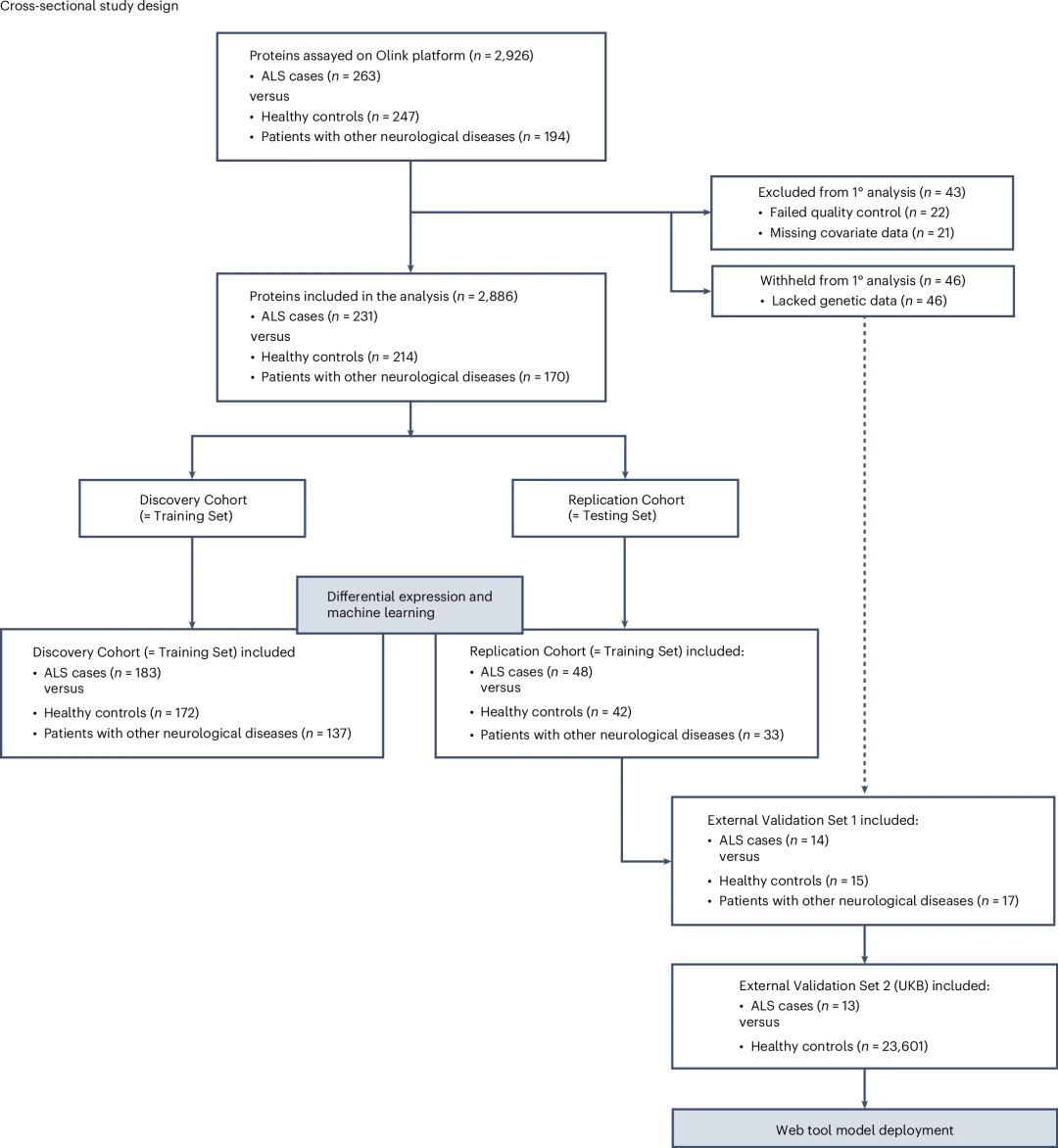
图1.研究工作流程。
在发现队列中,研究团队通过全蛋白质组关联分析,结合年龄、性别、样本类型和人群分层等因素,发现了33种血浆蛋白在ALS中丰度显著改变。其中,差异丰度最高的蛋白是神经丝轻链(NEFL),已有研究显示该蛋白在ALS和多种神经系统疾病中升高。该分析发现的其余31种蛋白质此前并没有明确地与ALS关联,包括参与能量代谢、神经功能和肌肉维护的分子。研究团队通过ELISA和SomaScan 7K蛋白质组数据集的额外验证以及验证队列(48例ALS病例,75例对照)分析了上述鉴定的蛋白质丰度差异,一致性为0.83(图2)。
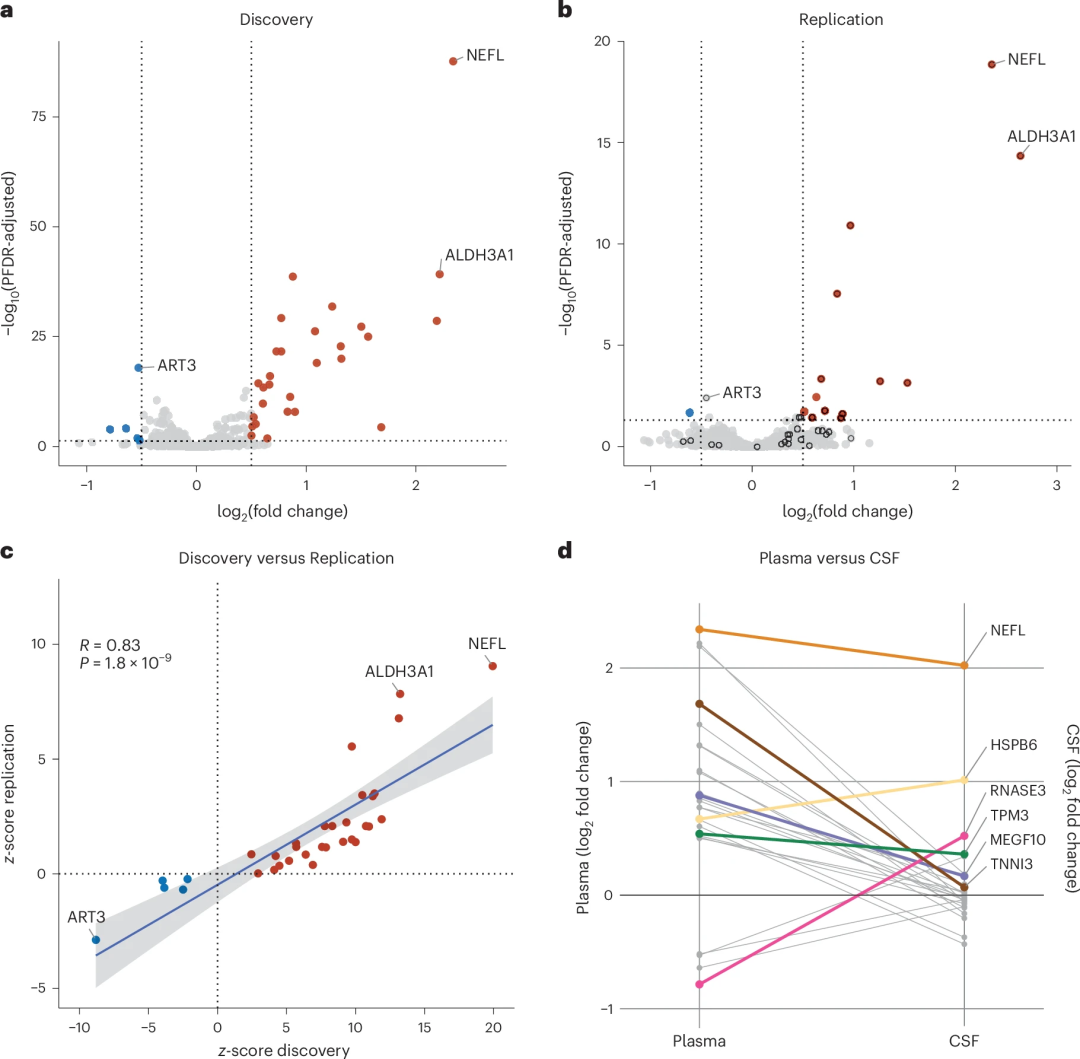
图2.与对照组相比,ALS患者血浆蛋白的丰度差异。
在血浆与脑脊液丰度差异蛋白的比较中,33种蛋白中的27种在SomaScan平台上进行了检测,其中5种蛋白(hspb6、MEGF10、NEFL、RNASE3和tpm3)在ALS患者脑脊液中显著升高(图2),其他蛋白在ALS患者脑脊液中无显著差异。
已知C9orf72扩增是ALS常见的一种遗传因素,研究团队通过分析C9orf72型ALS患者的血浆生物标志物,发现与非携带者相比,ALS C9orf72携带者中有8种蛋白显著上调。与对照组相比,ALS C9orf72携带者中同样的8种蛋白升高,表明这些8种蛋白的变化与C9orf72重复扩增有关。此外,在有症状C9orf72携带者中升高的特定蛋白(包括EIF2S2、HPCAL1、JPT2、MTIF3、PDAP1和SMAD3)在无症状携带者中没有明显变化,因此可能具有作为表型转化的生物标志物的潜力。
随后,研究人员对33种血浆蛋白的通路分析发现其与骨骼肌、神经元通路有较强的关联,强调了参与“骨骼肌发育和退化”、“能量代谢”等细胞通路的重要性。进一步多组学分析显示,ALS患者中观察到的丰度差异蛋白水平不是由其编码基因的变异直接驱动的。
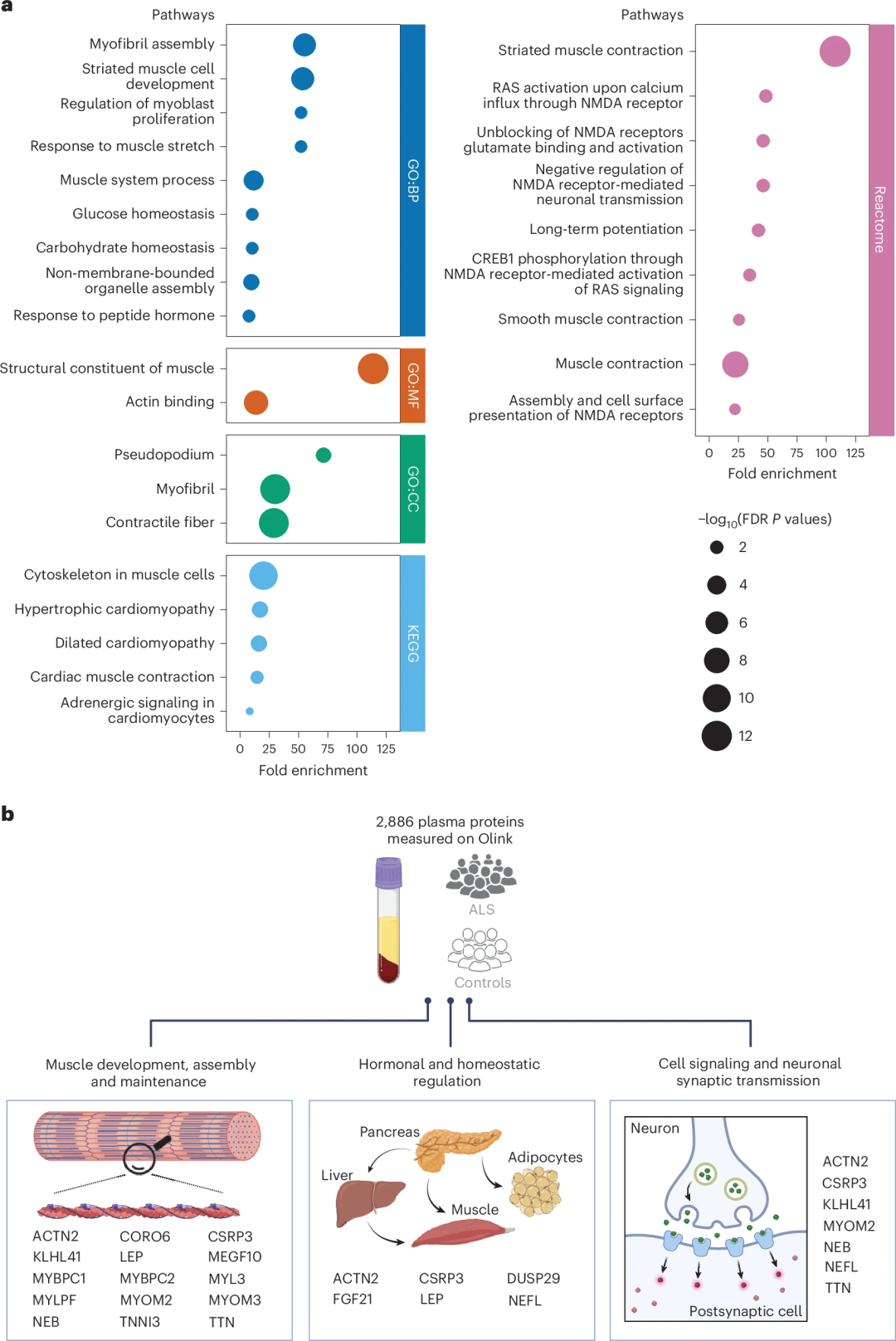
图3.基于丰度差异血浆蛋白的ALS通路分析。
研究团队评估了10种监督机器学习算法,在183例ALS病例和309例对照中进行训练。经比较分析,研究人员最终使用随机森林建立了整合蛋白质组和临床特征的诊断模型,并确定了20个特征(17种蛋白质、性别、采集样本时的年龄和血浆采集管)被确定为区分ALS病例与健康个体和其他神经系统疾病患者最具预测性的特征(图4a),AUC为96.2%;排除NEFL后,该模型AUC下降了约2.4%-13.2%,表明该模型性能并不完全依赖于NEFL。在外部验证队列中,包括NIH检测的46个样本和来自UKB超过23,000人,该模型AUC超过了99%。
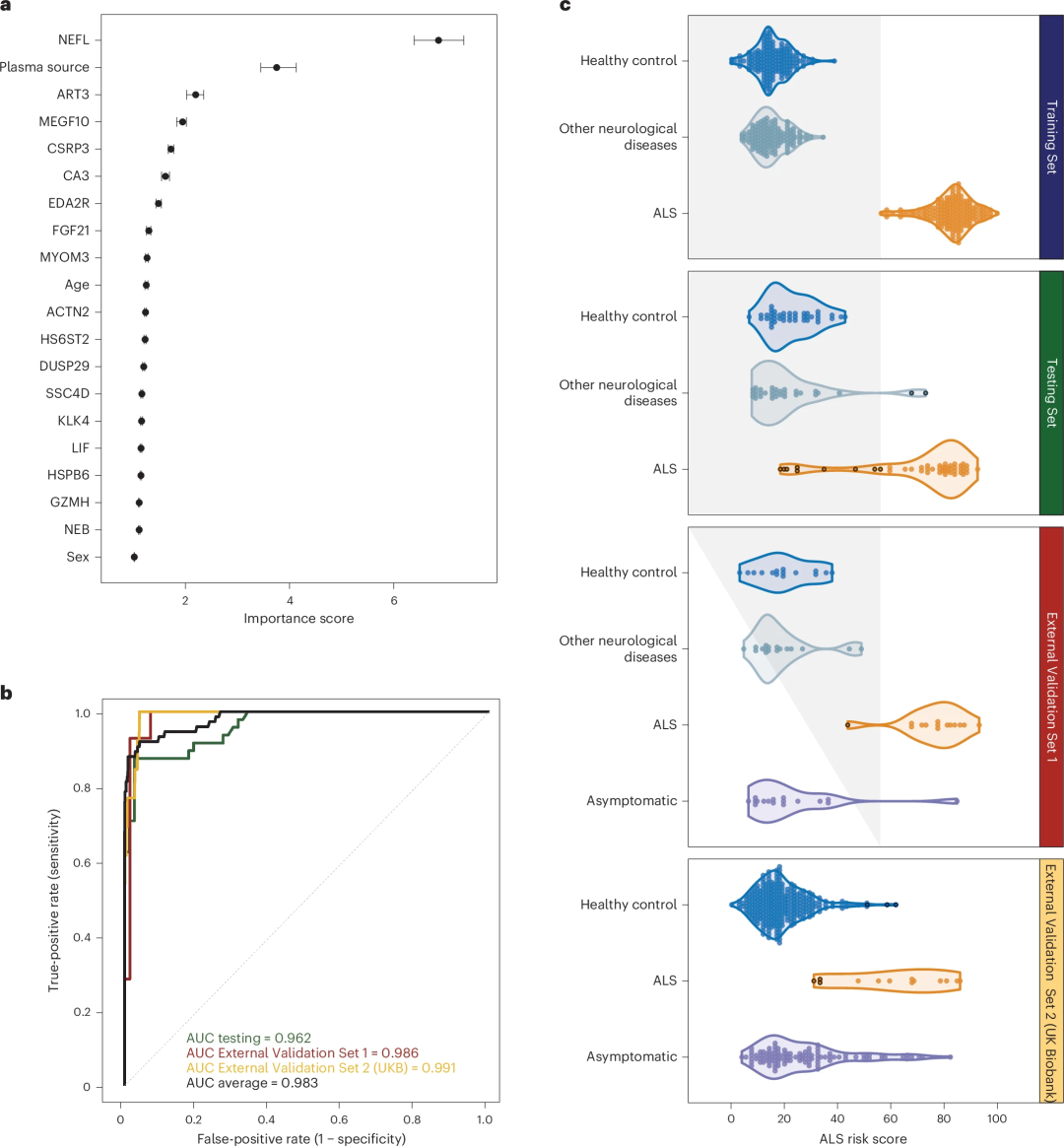
图4.基于血浆蛋白的ALS诊断模型。
最后,研究团队利用在ALS症状出现之前采集血浆样本的个体(从血浆采样到症状出现的平均持续时间= 6.4年)的数据来检测该模型在预估症状发作时间的性能(图5)。结果显示,ALS风险评分与症状出现时间存在显著相关性。ALS风险评分在症状出现前10年就开始发生变化,随着患者接近症状出现,该评分逐渐升高,在发病前5年左右达到50%。值得注意的是,ALS风险评分的增加并不是由于年龄的增加,因为患有其他神经系统疾病的个体、健康个体甚至是接受诊断后的ALS患者都没有表现出相同的趋势。分析发现,在无症状个体和ALS患者中,该模型的10种蛋白质分别与症状出现的时间相关(图5b),阳性系数最高的蛋白为NEFL,其次为CSRP3。
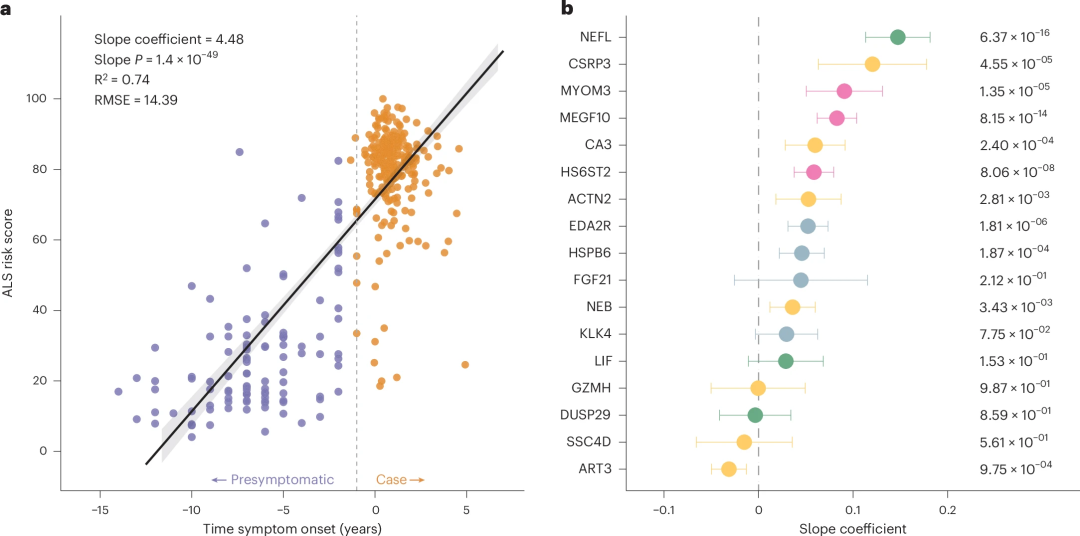
图5.诊断模型计算的ALS风险评分预估无症状患者的发病年龄。
结 语
迄今为止,ALS生物标志物的开发主要依赖于单一标志物的分析。该研究确定了ALS患者血浆中的蛋白质组可以作为生物标志物,能够以高特异性和敏感性将ALS患者与健康个体和其他神经系统疾病患者区分开。同时,该研究还证明了新构建的机器学习模型计算的ALS风险评分可以用作预测个体可能出现ALS症状的年龄。此外,基于血液的检测不仅能够促进ALS的早期评估,还有助于简化临床检测,降低成本和患者的负担。
原文信息:
Chia, R., Moaddel, R., Kwan, J.Y. et al. A plasma proteomics-based candidate biomarker panel predictive of amyotrophic lateral sclerosis. Nat Med (2025). https://doi.org/10.1038/s41591-025-03890-6


