【骨麻征途】舒更葡糖 (sugammadex) 的体外及全髋关节置换术后免疫调节作用:一项随机对照预试验和回顾性队列研究
时间:2025-08-29 12:15:20 热度:37.1℃ 作者:网络

摘要
背景(BACKGROUND) 术后免疫抑制是一种众所周知的现象,与感染性并发症相关。围术期免疫失调可能由手术损伤和麻醉药物诱发,但其特征远未得到全面阐明。为解决此问题,必须探究单个药物对免疫功能的影响。舒更葡糖 (Sugammadex) 是一种可封装罗库溴铵 (rocuronium) 的环糊精,也能结合其他药物和结构,并可能影响炎症反应。
目的(OBJECTIVE) 研究舒更葡糖潜在的免疫调节作用。
设计(DESIGN) 一项体外实验、随机对照预试验和回顾性队列研究。
机构(SETTING) 三级教学医院。
患者(PATIENTS) 12 名健康捐献者,20 名接受全髋关节置换术的成人,以及 1000 名接受腹部大手术的患者。
干预(INTERVENTION)
体外实验:分离的外周血单核细胞在用人源大肠杆菌脂多糖(LPS) 刺激前,暴露于舒更葡糖和罗库溴铵。
预试验:在单次脊髓麻醉下接受全髋关节置换术的患者,在手术结束时随机接受舒更葡糖(8 mg kg^{-1}−1) 或安慰剂。
主要结局指标(MAIN OUTCOME MEASURE)
体外实验:TNF、IL-1β 和 IL-6 的产生能力。
预试验:全血经LPS 刺激后的离体细胞因子产生能力。
回顾性队列:舒更葡糖作为术后感染性并发症的预测因子。
结果(RESULTS)
体外实验:罗库溴铵抑制了TNF 和 IL-1β 的产生能力。较高剂量的舒更葡糖 (100 和 1000 µg ml^{-1}−1,100 µg ml^{-1}−1 相当于给予 8 mg kg^{-1}−1 舒更葡糖后达到的血浆浓度) 恢复了 TNF 和 IL-1β 的抑制。
预试验:在手术结束时或术后第1 天,舒更葡糖组和安慰剂组之间的离体细胞因子产生能力无差异。
回顾性队列研究:舒更葡糖与术后感染性并发症无关联(OR = 1.000, 95% CI 0.998 至 1.002)。
结论(CONCLUSION) 舒更葡糖在体外保留了 TNF 和 IL-1β 的细胞因子产生能力。临床预试验和回顾性队列研究未显示舒更葡糖在临床使用剂量范围内具有术后早期免疫调节作用。
引言
术后感染仍然是手术后最常见的并发症之一,患病率在4% 到 10% 之间。由于其与死亡率、发病率和住院时间延长相关,它们对患者和医疗系统都产生了重大影响。尽管关节置换术后的感染率较低,但假体周围关节感染是一种毁灭性的并发症,导致严重的残疾。因此,降低这种并发症的风险至关重要。
通过改善与手术操作相关的因素,如无菌工作条件和实施快速通道手术,已经实现了术后感染的减少和更快的恢复。然而,消除术后感染的挑战仍然存在。在这方面,近期的焦点已转向理解免疫系统对手术的生理和病理生理反应。手术创伤诱导受损细胞释放损伤相关分子模式(DAMPs)。DAMPs 与抗原呈递细胞上的模式识别受体结合,启动细胞因子释放级联反应。肿瘤坏死因子 (TNF) 和白介素 (IL)-1β 在创伤或手术后不久升高,并激活其他促炎介质如 IL-6,但也激活抗炎介质如 IL-10。由于伴随的促炎和抗炎反应导致的免疫稳态失调被认为是术后感染性并发症的关键因素。 在创伤患者中,TNF 血浆水平升高以及 TNF 和 IL-1β 的离体细胞因子反应性下降与多器官功能障碍综合征相关。在腹部手术患者中,发现感染性并发症与术后 TNF 和 IL-1β 的离体细胞因子产生能力下降之间存在关联。
阐明对抗这种免疫抑制状态的方法很困难。减少手术创伤,例如通过腹腔镜手术,被认为可以限制炎症和抗炎反应。此外,不同的术中麻醉药物被认为对免疫反应产生不同的影响,但单个药物的效果远未得到全面表征,需要探索。然而,在围术期临床试验中分离或控制这些潜在的免疫影响因素具有挑战性。
舒更葡糖是一种改良的γ-环糊精,通过封装非去极化神经肌肉阻滞剂 (NMBAs) 来逆转神经肌肉阻滞。然而,舒更葡糖可以结合其他细胞结构,尽管亲和力较低。例如,在先前对动物模型的研究中发现,舒更葡糖可能对神经炎症过程产生限制作用并具有抗炎作用。因此,舒更葡糖可能具有延伸效应,并可能影响炎症反应。
因此,本研究探讨了舒更葡糖潜在的积极免疫调节影响。通过一项体外研究初步评估了舒更葡糖的效果。随后的一项临床预试验研究了在椎管内麻醉下全髋关节置换术(THA) 结束时使用舒更葡糖对术后免疫抑制的影响。还进行了一项回顾性队列研究,以评估舒更葡糖给药对腹部大手术后 30 天并发症的影响。
材料与方法
首先,进行了一项体外实验,以评估单独暴露于舒更葡糖以及与罗库溴铵联合使用时的免疫调节作用。在体外实验之后,进行了一项临床预试验以进一步评估舒更葡糖的效果。该预试验是一项在拉德堡德大学医学中心(荷兰奈梅亨)进行的单中心、随机对照预试验。获得了医学研究伦理委员会'METC Oost-Nederland' (NL82808.091.22, 2023年1月25日) 和主管当局的许可。所有个体在研究参与前均提供了书面知情同意。本手稿遵循适用的 CONSORT 指南。最后,对一项回顾性队列研究进行了事后分析,以评估临床预试验的结果。
体外实验(In-vitro experiment)
在体外实验中,从健康捐献者分离的外周血单核细胞(PBMCs) 在用大肠杆菌 (E. coli) 脂多糖 (LPS) 刺激之前,暴露于舒更葡糖和罗库溴铵。之后,量化细胞因子产生能力以评估免疫细胞的功能。
在获得书面知情同意后,从12 名健康志愿者的血样中获得白细胞层(荷兰桑奎恩血库,奈梅亨)。PBMCs使用密度梯度离心法通过 Ficoll-Paque (GE Healthcare, Uppsala, Sweden) 从白细胞层中分离出来。随后,用 4°C 的磷酸盐缓冲盐水洗涤三次。之后,将 PBMCs 重悬于细胞培养基 [Roswell Park Memorial Institute (RPMI) 1640 Dutch Modified (Gibco, Thermo Fisher Scientific, Waltham, MA, USA)] 中,并补充庆大霉素 50 µg ml^{-1}−1、丙酮酸盐1 mmol l^{-1}−1 和 GlutaMAX 2 mmol l^{-1}−1。此后,将重悬的PBMCs 在 96 孔圆底板中培养,每孔 5 x 10^55 个细胞,并与仅培养基或罗库溴铵 (0.5, 5, 15, 50 和 100 µmol l^{-1}−1) 一起孵育一小时 。之后,再用培养基或舒更葡糖 (10, 100 和 1000 µg/ml) 进行另一次 1 小时的孵育,导致细胞仅与培养基(阴性对照)、罗库溴铵、舒更葡糖或组合一起孵育。孵育后,用 10 ng ml^{-1}−1 大肠杆菌 (血清型 O55:B5; Sigma Aldrich, St Louis, Missouri, USA) 刺激细胞 24 小时,以评估免疫细胞的功能。刺激 24 小时后,离心样品 (1400 RPM,室温,8 分钟),并将上清液在 -20°C 下储存直至分析。
为了评估与舒更葡糖和罗库溴铵孵育后的免疫细胞功能,在上清液中测定了细胞因子浓度[TNF, IL-6, IL-18]。这是分批使用 ELISA 按照制造商的说明 (R&D systems, Minneapolis, Minnesota, USA) 进行的。
临床预试验(Clinical pilot study)
在临床预试验中,在椎管内麻醉下THA 结束时给予舒更葡糖,以研究在无罗库溴铵的情况下对术后先天免疫功能的影响。由于本研究是一项预试验,未进行样本量计算。计划纳入 20 名患者,基于类似的研究。[13,16,21,22]
参与者(Participants)
要符合研究参与资格,患者必须年满18 岁,并计划在椎管内麻醉下接受初次 THA。排除标准包括:荷兰语掌握不足,无法理解患者信息并填写问卷;使用舒更葡糖或琥珀胆碱的禁忌症;维生素 K 依赖性凝血因子缺乏或凝血病;严重肾脏(肌酐清除率 < 30 ml min^{-1}−1) 或肝脏疾病(Child-Pugh 分级 C);以及长期使用精神药物、NSAIDs、类固醇或免疫抑制药物。此外,我们排除了怀孕、目前正在哺乳或具有生育潜力但未使用充分避孕措施的妇女。最后,我们排除了因智力受损而无法做出知情选择或同意的患者。患者由其治疗骨科医生筛选资格。
随机化和盲法(Randomisation and blinding)
手术前不久,患者被随机分配到干预组或对照组。干预组在手术结束时接受舒更葡糖8 mg kg^{-1}−1,对照组则接受安慰剂(0.9% NaCl)。计算机生成的随机化由 Castor EDC (Castor Electronic Data Capture) 以 1:1 的方式和可变的区组大小随机化进行,以隐藏分配。未进行分层。患者和所有人员对治疗分配设盲,包括麻醉师及其助手。研究药物由一位不参与结果评估的未设盲研究医生给药,以确保患者和人员的盲态。由于未发生紧急情况,无需揭盲。
麻醉和手术(Anaesthesia and surgery)
椎管内麻醉,即单次脊髓麻醉,使用0.5% 布比卡因 10 至 20 mg 联合舒芬太尼获得。如果患者偏好,可通过输注丙泊酚 1.5 至 4.5 mg kg^{-1}−1 h^{-1}−1 获得额外镇静。根据当地方案,患者术前接受扑热息痛、抗坏血酸和普瑞巴林作为预用药。此外,术中给予艾氯胺酮。避免使用地塞米松,以防止对术后免疫结局测量的影响。THA 通过后外侧入路并使用骨水泥假体进行。在手术结束时,皮肤缝合期间给予研究药物。
结局指标(Outcomes)
本试验的主要结局是通过全血刺激后的离体细胞因子产生能力反映的术后先天免疫功能。在三个时间点采集血样:术前、给予研究药物后以及术后第1 天。全血在体外用大肠杆菌 LPS 刺激,方法与体外实验相同,并在别处描述。简言之,将 0.5 ml 全血加入含有 2 ml 培养基的试管(阴性对照)或含有补充了 12.5 ng ml^{-1}−1 大肠杆菌 LPS(最终浓度 10 ng ml^{-1}−1,血清型O55:B5; Sigma Aldrich)的培养基的试管中。试管孵育 24 小时(37°C,5% CO_22),然后离心(室温3800 RPM 10 分钟)。LPS 刺激后的上清液在 -80°C 下储存直至分析。为了评估免疫系统的功能,使用 Human Bio-Technic R&D ELISAs 按照制造商的说明 (R&D systems, Minneapolis, Minnesota,美国,目录号DY206, DY201, DY210 和 DY217B) 分批测定细胞因子浓度 (TNF, IL-6, IL-18, IL-10)。
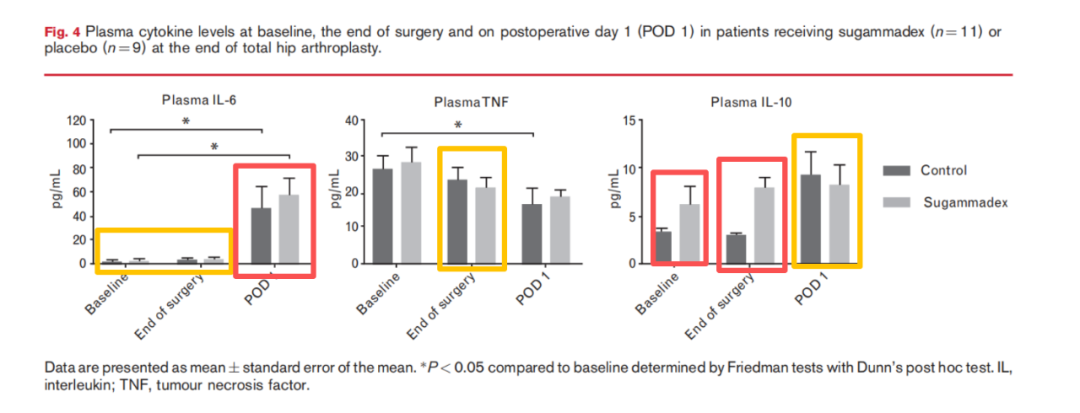
次要结局包括通过测量三个不同时间点所获血样中的循环炎症细胞因子进一步评估先天免疫功能。将锂肝素和EDTA 采血管中获取的血样离心(室温 3800 RPM 10 分钟),EDTA 样品再次离心 [16,000 相对离心力 (RCF),室温 10 分钟]。之后,血浆样品在 -80°C 下储存直至分析。使用 Luminex 检测法按照制造商的说明 (Milliplex; Millipore, Billerica, Massachusetts, USA) 分批测量促炎和抗炎细胞因子 (TNF, IL-6, IL-10) 的血浆浓度。
其他次要结局包括健康相关生活质量、疼痛感知和术后并发症。健康相关生活质量通过经过验证的恢复质量-40 (QoR-40) 问卷进行评估,由患者在术前和术后第 1 天填写。此外,在麻醉后监护室 (PACU) 和术后第 1 天通过数字评分量表 (NRS; 0 至 10) 评估疼痛感知。根据 Clavien-Dindo 分类,将术后最多 30 天的并发症登记为标准护理的一部分。感染性并发症根据 StEP-COMPAC 小组倡议的标准进行评分。
回顾性队列分析(Retrospective cohort analysis)
为了评估临床预试验的结果,我们对一项近期发表的关于腹部大手术后早期术后疼痛和30 天并发症的回顾性队列研究进行了事后分析。该研究包含了 2014 年 1 月至 2020 年 12 月期间在拉德堡德大学医学中心接受手术的 1000 名患者。纳入的手术包括食管手术、肝脏手术、胰腺手术以及细胞减灭术和腹腔热灌注化疗 (HIPEC)。对所有患者,根据疾病控制中心对医疗保健相关感染的定义对术后 30 天感染进行评分。数据收集的完整方法学解释可在原始研究中找到。除了已发布的数据外,该数据库还包含每位患者的舒更葡糖给药数据。研究了舒更葡糖给药与术后感染性并发症之间的潜在关联。
统计分析(Statistical analysis)
体外实验的细胞因子产生能力通过与对照比较,使用Friedman 检验和 Dunn 事后检验(非正态分布)进行分析。在 THA 的临床预试验中,组间细胞因子产生能力和血浆细胞因子的差异使用 Mann–Whitney U 检验进行比较,随时间变化的差异使用 Friedman 检验和 Dunn 事后检验进行比较。两组之间基线特征的变异使用标准化差异进行比较。根据样本量计算,标准化差异 (ASD) 大于 0.66 的变量被认为不平衡。 对于其他次要结局,正态分布的连续数据使用 Student’s t 检验,非正态分布数据使用 Mann–Whitney U 检验。分类数据通过 χ² 检验进行比较。P 值小于 0.05 被认为具有统计学意义。由于本研究规模较小且具有探索性质,未对多重检验进行校正。所有分析均基于意向治疗原则,且未对缺失数据进行插补。
对于事后回顾性队列分析,使用多变量逻辑回归来研究舒更葡糖给药与术后30 天感染性并发症之间是否存在关联。在此分析之前,首先逐个测试潜在的解释变量,如果 P 值小于 0.05,则将其纳入多变量逻辑回归模型。将舒更葡糖添加到多变量逻辑回归模型中,以评估其相对于其他解释变量的效果。使用 SPSS 软件 (SPSS V.27.0, IBM, Released 2020, Armonk, New York, USA) 进行统计分析。
结果
体外实验(In-vitro experiment)
体外实验表明,与阴性对照相比,在LPS 刺激前仅用罗库溴铵孵育会导致细胞因子产生能力的剂量依赖性抑制,如图 1a 所示。对于 5, 15, 50 和 100 µmol l^{-1}−1 的罗库溴铵浓度,TNF 和 IL-1β 的减少是显著的,并且在最高浓度下 IL-6 也显著减少。通过细胞毒性试验评估,罗库溴铵不影响细胞活力。
在LPS 刺激前仅用舒更葡糖孵育显示了对 TNF 的有趣的剂量依赖性趋势。在较低剂量下,它降低了 TNF 产生能力,而在较高剂量下,它增加了 TNF 产生能力。单独使用舒更葡糖似乎不影响 IL-1β 和 IL-6 的产生能力。进一步分析显示,对于罗库溴铵和舒更葡糖的组合,高剂量的舒更葡糖 (100 和 1000 μg ml^{-1}−1) 抵消了罗库溴铵对 TNF 和 IL-1β 产生的抑制。
临床预试验(Clinical pilot study)
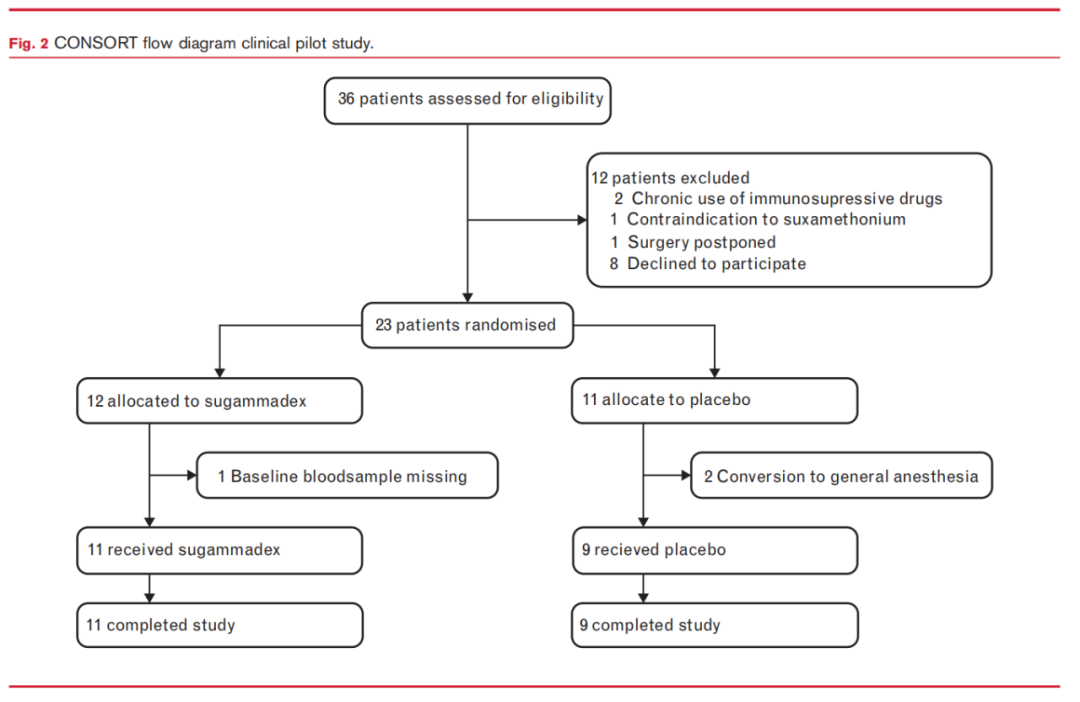
临床预试验于2023 年 3 月至 2023 年 10 月期间进行,对 36 名患者进行了资格评估。
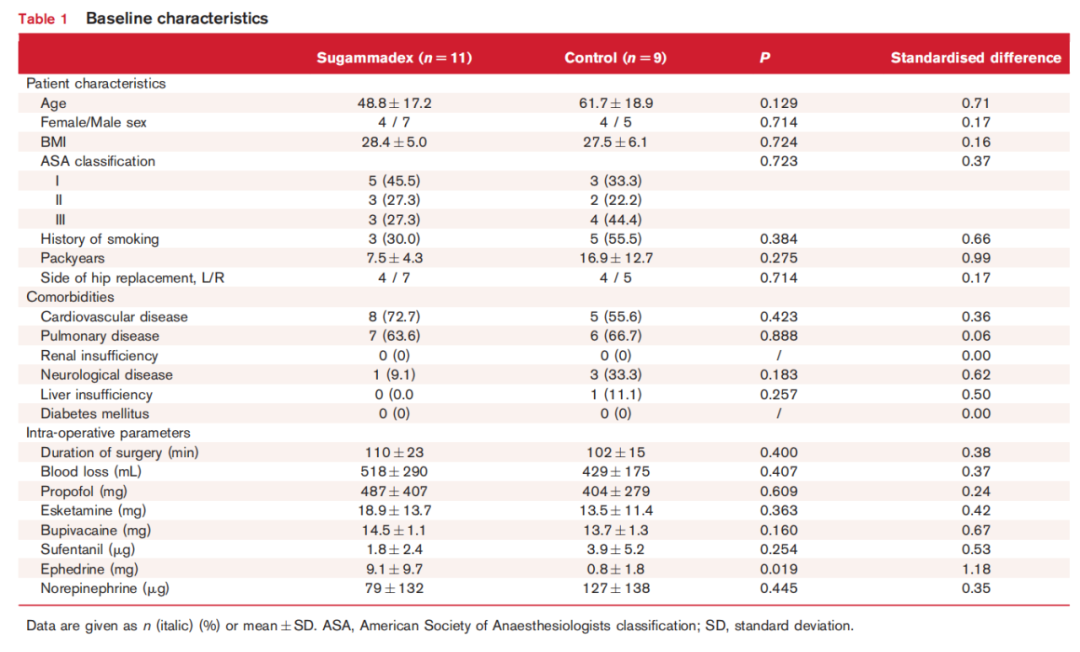
最终随机化了23 名患者,而非最初计划的 20 名入组者,因为有 3 名患者在随机化后被排除和替换。具体而言,两名患者在手术室中被认为无法进行椎管内麻醉,一名患者无法获取血样。其余 20 名患者完成了研究。两组之间的基线特征和术中参数相似,见表 1。
先天免疫功能(Innate immune function)
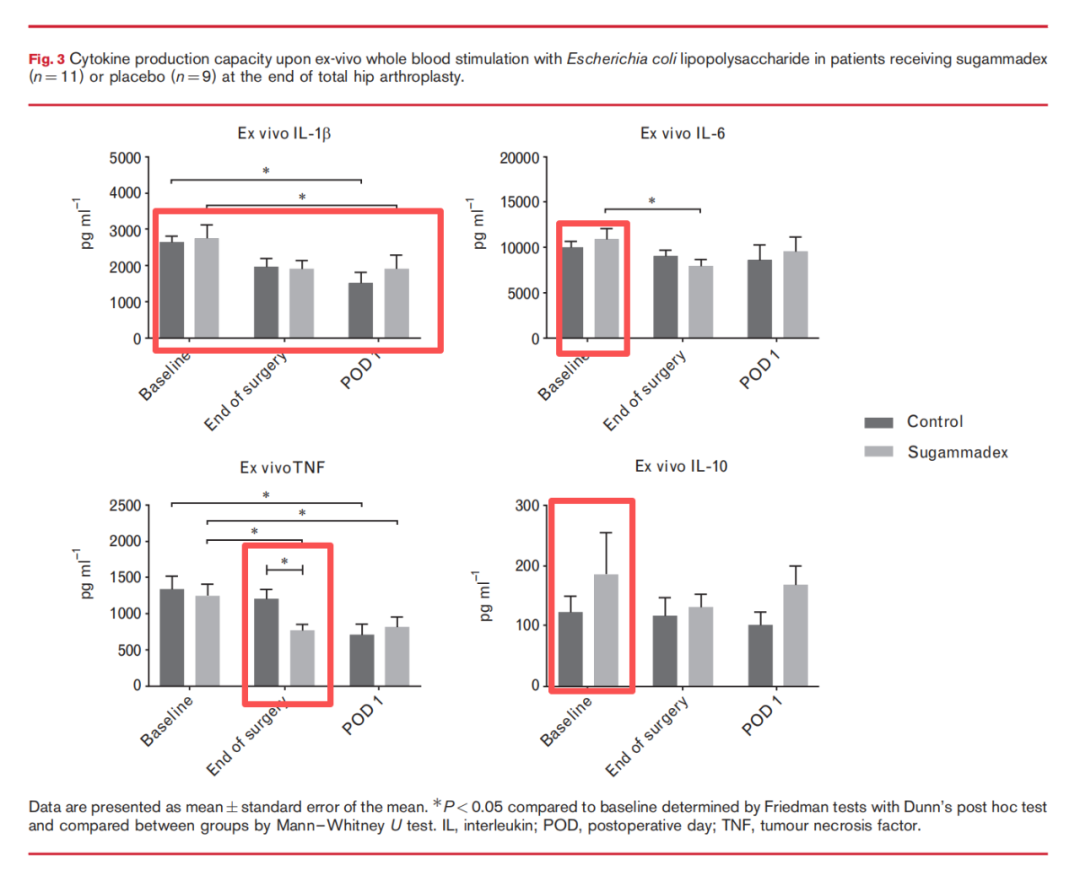
总体而言,舒更葡糖组和安慰剂组之间刺激后的细胞因子产生能力随时间推移没有差异(图3)。两组中,术后第 1 天 (POD 1) 的 TNF 和 IL-1β 产生能力与基线相比显著下降,证实了手术后的免疫抑制。在手术结束时,安慰剂组的 TNF 似乎比舒更葡糖组保留得更好(舒更葡糖 768 ± 318 pg ml^{-1}−1 对比 安慰剂 1196 ± 412 pg ml^{-1}−1, P = 0.025P=0.025)。这种差异在术后第 1 天消失。至于 IL-10 和 IL-6,未观察到随时间变化的趋势。
临床结局(Clinical outcomes)
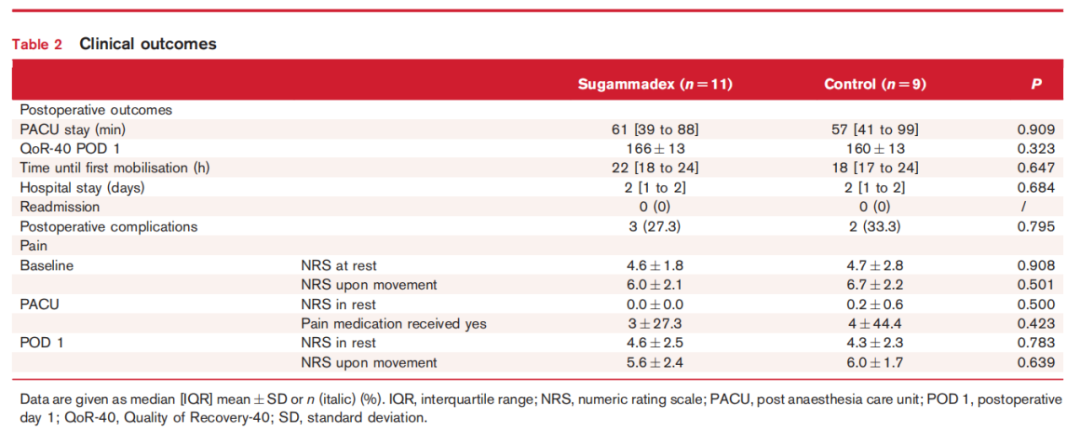
总体而言,干预组和对照组之间的临床结局未观察到统计学显著差异,如表2 所示。术后第 1 天,舒更葡糖组与安慰剂组的平均恢复质量-40 (QoR-40) 评分分别为 166 ± 13 对比 160 ± 13 分 (P = 0.323)。术后第一天的平均疼痛评分在舒更葡糖组和对照组之间没有差异(静息时 NRS 4.6 ± 2.5 对比 4.3 ± 2.3, P = 0.783),(活动时 NRS 5.6 ± 2.4 对比 6.0 ± 1.7, P = 0.639)。本研究登记了 5 例并发症,其中 4 例被归类为 Clavien-Dindo I 级,无需任何治疗。对照组中的一名患者因浅表伤口感染接受了抗生素治疗。
回顾性队列分析(Retrospective cohort analysis)
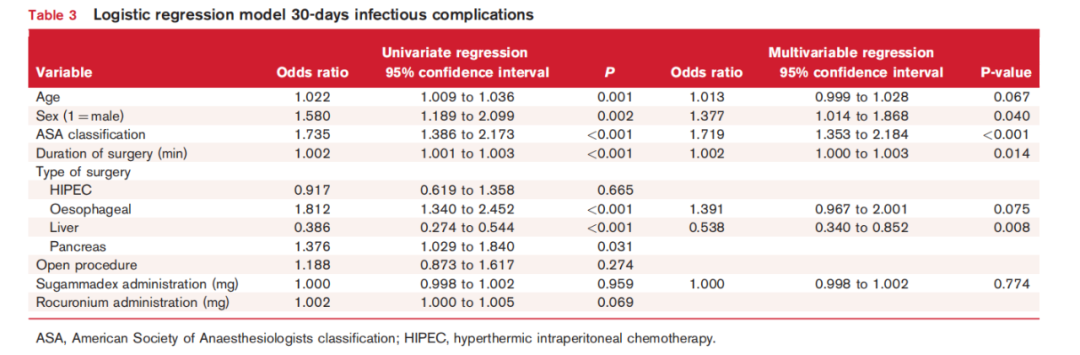
在回顾性队列研究的1000 名患者中,186 名患者接受了舒更葡糖,平均剂量为 170 ± 77.5 mg。共有 289 名患者发生了感染性并发症。单变量逻辑回归分析显示,舒更葡糖给药不是术后 30 天感染性并发症的显著预测因子 (OR = 1.000, 95% CI 0.998 至 1.002, P = 0.959)(表 3)。多变量回归分析证实了这一点。此外,罗库溴铵也不是术后 30 天感染性并发症的显著预测因子 (OR = 1.002, 95% CI 1.000 至 1.005, P = 0.069)。
讨论
本研究调查了舒更葡糖对先天免疫系统的影响。体外实验表明,与罗库溴铵的免疫抑制作用相反,舒更葡糖保留了TNF 和 IL-1β 的产生能力。然而,我们未能在接受 THA 的患者中证实舒更葡糖在临床剂量范围内有任何术后免疫调节作用。
舒更葡糖是一种改良的γ-环糊精,专门设计并引入用于其封装 NMBAs 以逆转神经肌肉阻滞的能力。这种能力导致神经肌肉阻滞的恢复显著加快,使舒更葡糖能够迅速适应常规实践。尽管其主要功能是封装 NMBAs,但舒更葡糖表现出结合或封装其他结构的能力,尽管亲和力较低。在存在 NMBAs 的情况下,置换相互作用很少见。然而,在舒更葡糖过量、游离形式舒更葡糖水平升高或不存在 NMBAs 的条件下,与其他药物或分子的相互作用是可能的,可能引起免疫调节作用。 例如,由于与 NMBAs 的结构相似性,类固醇也可以结合舒更葡糖,并且有报道称舒更葡糖给药后类固醇浓度降低。 然而,这些反应的真实程度及其临床相关性仍然存在争议。
为了更详细地探索舒更葡糖的这些潜在免疫调节作用,我们进行了一项结合基础研究、临床预试验和回顾性队列研究的研究。最初的体外实验为舒更葡糖的免疫调节作用提供了证据。使用了10、100 和 1000 µg ml^{-1}−1 的不同剂量舒更葡糖,分别对应于预计给予 2、8 和 64–96 mg kg^{-1}−1 舒更葡糖后的血浆浓度。尽管体外实验的结果令人鼓舞,但在预试验中未观察到免疫调节作用。给予的剂量为 8 mg kg^{-1}−1,这在日常实践中被认为是相对较高的,但可能不足以引起可观察到的效应。在体外实验中,最高浓度与细胞因子产生能力的显著提升相关,但该剂量远远超过了典型的临床剂量。此外,体外刺激实验的性质是将固定浓度的舒更葡糖作用于细胞24 小时,这并不能精确模拟患者体内随时间变化的血浆浓度,因为舒更葡糖的半衰期约为 2 小时。另外,体内血浆浓度由于药效动力学过程是动态的,这给直接将临床给药剂量转化为体外浓度带来了挑战。尽管这些复杂性强调了将基础研究转化为临床结果的局限性,但本研究中将两种方法结合使用,提供了对舒更葡糖对免疫系统潜在影响的见解。
临床预试验的结果显示,术后第1 天 IL-1β 和 TNF 的产生能力与基线相比显著降低。这表明存在免疫抑制状态,与先前关于术后免疫失调的发现一致。据认为,与创伤类似,组织损伤通过危险相关分子模式和模式识别受体启动伴随的促炎和抗炎反应。^{40}40 预试验中观察到的术后第 1 天血浆 IL-6 水平升高支持了这一点。对抗这种免疫失调的策略令人感兴趣。然而,本研究表明,舒更葡糖似乎不太可能具备在日常实践使用的剂量下解决这种失调的能力。
除了研究舒更葡糖的影响外,体外实验还提供了关于罗库溴铵对免疫功能潜在影响的见解。值得注意的是,它揭示了罗库溴铵孵育后TNF 和 IL-1β 产生能力的剂量依赖性降低。单次给予 0.9 mg kg^{-1}−1 的罗库溴铵会导致峰值血浆浓度约为 12,000 ng ml^{-1}−1(相当于22.6 µmol l^{-1}−1),持续输注期间的稳态血浆浓度约为1000 至 2000 ng ml^{-1}−1(相当于1.9 至 3.8 µmol l^{-1}−1)。细胞因子产生能力的下降可能通过罗库溴铵与烟碱型乙酰胆碱受体(nAch) 的竞争性结合来解释。这些受体也存在于免疫细胞上,包括巨噬细胞、树突状细胞和淋巴细胞。例如,α7 nACh 亚基在胆碱能抗炎通路中起重要作用,该通路调节免疫细胞增殖、T 细胞分化、抗原呈递和细胞因子产生。因此,罗库溴铵的竞争性结合可能诱导免疫失调。然而,由于我们未在临床研究中研究罗库溴铵的效果,因此必须像对待舒更葡糖结果一样谨慎对待这些结果。需要进一步的研究来探索这个潜在问题。
通过整合体外实验、临床预试验和回顾性队列研究,本研究增强了我们对该主题的理解。体外实验解释的困难和局限性通过直接回答临床环境中舒更葡糖的免疫调节作用得到了弥补。本研究的另一个优势在于在预试验中消除了罗库溴铵的影响。这使我们能够得出结论,观察到的舒更葡糖效果的缺乏不仅仅是NMBAs 的伴随效应。然而,本研究的一个局限性是,在体外实验中,LPS 刺激是在 PBMCs 上进行的,而在临床预试验中是在全血上进行的,这限制了对绝对数值的直接比较。此外,体外研究 PBMCs 并未体现炎症反应的所有组成部分,尽管 PBMCs 在先天免疫反应的早期阶段至关重要。在结合的体外和临床研究中,我们专注于单核细胞响应病原体的受影响能力,并观察趋势的差异。我们认为,这些局限性并不妨碍研究体外实验和临床研究之间趋势差异的能力。另一个局限性是我们仅关注舒更葡糖和罗库溴铵,未研究其他神经肌肉阻滞剂或逆转剂,因此无法就肌肉松弛管理得出广泛的结论。鉴于本研究的样本量小和探索性质,我们选择不对多重检验进行校正。这一决定增加了假阳性结果的风险。然而,这种担忧主要适用于体外实验,这是唯一产生阳性结果的部分。两项实验的结合使我们质疑那些阳性结果,并得出结论:舒更葡糖似乎不太可能具有临床相关的免疫调节作用。在体外实验中观察到的罗库溴铵的效果仅凸显了需要进一步研究麻醉药物对术后免疫反应的影响。
结论
这项结合了体外实验、临床预试验和回顾性队列研究的研究表明,高剂量的舒更葡糖在体外保留了TNF 和 IL-1β 的产生能力。临床预试验显示,在接受 THA 的患者中,舒更葡糖在临床使用剂量范围内对细胞因子产生能力没有术后免疫调节作用。回顾性队列研究证实了这一点,因为在接受腹部大手术的患者中未观察到舒更葡糖对术后感染性并发症的影响。
骨麻征途 点评
该项研究通过多层次的研究设计,综合探讨了舒更葡糖的免疫调节作用。其体外实验发现,罗库溴铵会抑制免疫细胞的炎性细胞因子(TNF, IL-1β)产生能力,而高浓度的舒更葡糖(100及1000 µg ml⁻¹)能够逆转这种抑制效应。然而,在随后的临床随机对照预试验中,在接受全髋关节置换术的患者体内,临床常用剂量(8 mg kg⁻¹)的舒更葡糖并未表现出任何显著的术后免疫调节作用,治疗组与安慰剂组在细胞因子产生能力、血浆炎症指标及临床康复结局上均无差异。这一阴性结果在一项纳入1000名腹部大手术患者的回顾性队列研究中得到进一步证实,分析显示舒更葡糖的使用与术后感染并发症的风险无关。综上所述,该研究表明,尽管舒更葡糖在极高浓度下于体外具有免疫调节潜力,但在临床常规剂量范围内,它并不会产生具有临床意义的免疫调节效应。


