【BJH】双抗治疗淋巴瘤的患者评估、治疗实施和毒性管理:英国血液学学会良好实践文件
时间:2025-09-10 12:14:07 热度:37.1℃ 作者:网络
双特异性抗体(BsAb)是一类新型药物,通过共同靶向肿瘤抗原和T细胞或自然杀伤细胞,以不依赖于Fcγ受体和主要组织相容性复合物的方式激活内源性免疫细胞。抗CD3×CD20 BsAb在经深度治疗的B细胞淋巴瘤患者中显示出显著活性,Epcoritamab、glofitamab(格菲妥单抗)、mosunetuzumab(莫妥珠单抗)和odronextamab均在R/R B细胞淋巴瘤(包括LBCL、FL和套细胞淋巴瘤)患者中显示出单药疗效。
英国血液学学会(BSH)制定了良好实践文件,基于目前经英国药品和健康产品管理局(MHRA)和/或欧洲药品管理局(EMA)批准的淋巴瘤(主要是弥漫大B细胞淋巴瘤[DLBCL]和滤泡淋巴瘤[FL])抗CD3×CD20 BsAb,为治疗相关的患者评估、治疗实施和毒性管理提供实用指导。本指南不包括这些抗体在 R/R LBCL 或 FL 治疗中的作用。

引言
CD3×CD20 BsAb关键研究中报告的针对获批适应症的总体缓解率(ORR)、完全缓解率(CR)、缓解持续时间(DoR)和完全缓解持续时间(DoCR)见表1。需要注意的是,由于患者人群不匹配,这些数据在研究间不能直接比较。但在所有适应症中,达到CR可意味着更长的DoR和无进展生存期(PFS)。
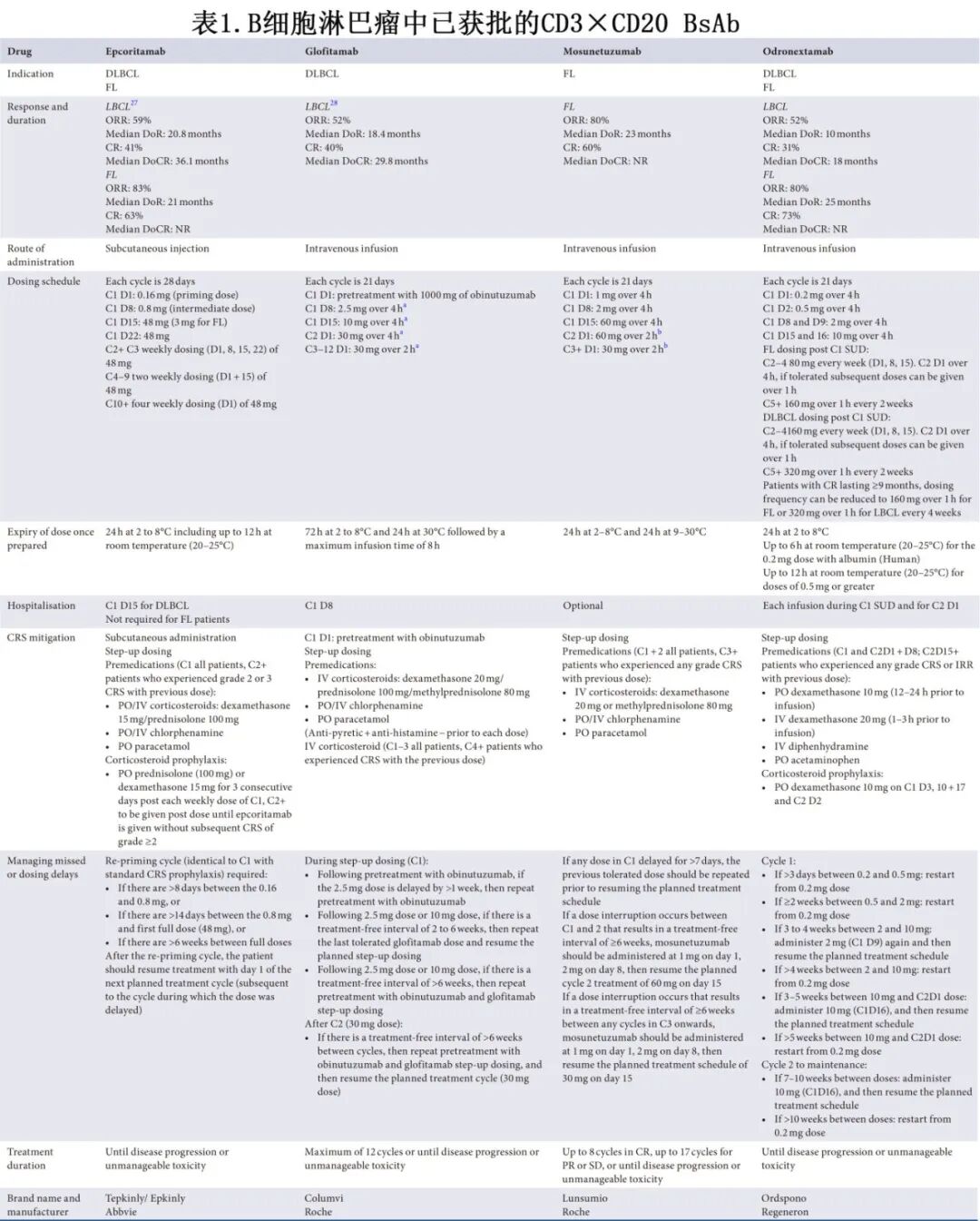
BsAbs目前正在与其他疗法联合用于复发难治性(R/R)LBCL和FL的研究,并显示出有希望的结果。此外,临床试验正在评估BsAbs在新诊断DLBCL和FL患者中的作用。
与CAR-T细胞疗法类似,BsAb治疗具有由免疫激活及随后B细胞耗竭介导的特征性且可预测的毒性谱。但BsAb治疗相关的细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)样神经毒性的发生率和严重程度要低。 BsAb的CRS发生时间也更可预测,总结在表2中。CRS通常发生在BsAb给药后1-2天内,持续1-3天,98%的事件会消退。CRS通常见于周期1的阶梯递增给药(SUD)期间,最常见于格菲妥单抗首次给药后(C1 D8)和epcoritamab首次全剂量给药后(C1 D15)。CRS有时在周期2中出现,但此后不常见。关键试验中任何级别CRS的发生率在39%至67%之间,其中约16%为2级CRS,<5%为≥3级CRS。据报道,33%的患者在后续给药中出现复发性CRS,通常为低级别,大多数为1级。
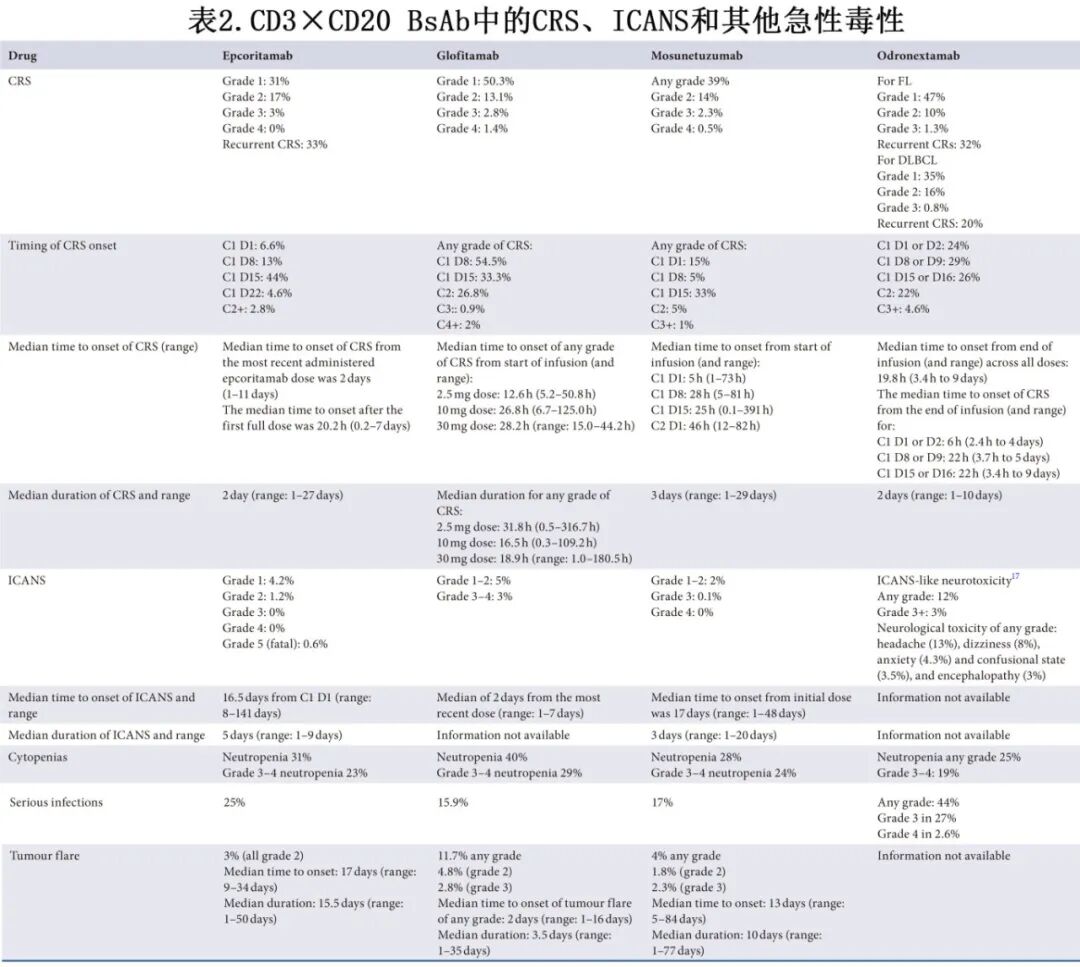
ICANS和ICANS样症状在BsAbs中比目前可用的CAR-T细胞产品少见得多。ICANS发生率、相对于剂量的中位发生时间和持续时间总结在表2中。关键试验中任何级别ICANS的频率在0%至8%之间,大多数事件为1级且具有自限性。格菲妥单抗报告了8%的任何级别ICANS样神经系统事件,其中≥3级事件占3%。epcoritamab报告了6%的任何级别ICANS(1级为4.2%,2级为1.2%,≥3级为<1%)。尽管ICANS的发生时间范围比CRS宽得多,但首次ICANS的中位时间通常在格菲妥单抗最近一次给药后2-3天内,以及epcoritamab和莫妥珠单抗在周期1 SUD期间首次全剂量给药后。94%的ICANS通过支持治疗可得到缓解。ICANS缓解的中位时间为2-3天(范围:1-20天)。
迄今为止,关于BsAb在R/R LBCL中真实世界经验的公开报道有限。对英国真实世界经验(RWE)的初步审查表明,安全性特征似乎与已公布数据相似,33%的患者发生CRS,15%为≥2级,17%的患者需要托珠单抗,4%出现ICANS,5%需要入住重症监护室(ICU)。然而真实世界的缓解率较低,可能反映出真实世界中选择了具有高度侵袭性疾病动力学和体能状态差的患者。需要继续收集RWE工作以识别可能无法从BsAb中受益的患者。
缓解这些毒性的策略,如SUD和皮质类固醇预用药,已常规纳入BsAb给药方案。重要的是,CD3×CD20 BsAb的另一个显著毒性为B细胞发育不全和感染风险增加。
尽管CAR T细胞疗法彻底改变了许多R/R B细胞淋巴瘤患者的结局,但由于物流、地理和资源限制,其可及性有限。在英国、欧盟和许多其他地区,CAR-T细胞输注仅限于特定的、拥有细胞治疗认证基金会(FACT)或联合认证委员会ISCT-Europe & EBMT (JACIE) 认证的大型造血干细胞移植中心。居住在远离CAR-T细胞输送中心的患者、社会经济地位较低的患者以及少数族裔社区接受CAR T细胞治疗的可能性较小。CAR-T细胞治疗的生产时间和生产失败的风险也是限制因素,多达25%的获批患者未能接受输注(主要是因为在等待CAR-T细胞生产期间疾病进展导致临床状况恶化),尽管英国的经验显示,随着时间的推移,接受输注的患者比例有所提高。相比之下,BsAb治疗具有“现货型”的优势,具有可管理的毒性特征,并且可以在较小的当地医院进行,而无需FACT/JACIE认证。然而,应该认识到,与BsAb相比,CAR-T细胞治疗具有更长期的随访数据,部分患者有可能实现治愈,而BsAb的长期疗效尚未确定。
采用BsAb治疗的一个重要步骤是开发针对这些产品的给药和毒性管理的健全途径。根据能力和当地情况,一些较小的医院可能与最近的转诊中心合作,在第1周期间进行SUD给药,因为此时CRS的风险最高。
患者评估和诊断
考虑接受BsAb治疗的患者应进行体能状态评估和基线血液检查,包括全血细胞计数、常规生化、血清乳酸脱氢酶、C反应蛋白(CRP)和血清免疫球蛋白(Ig)水平。如果怀疑有循环肿瘤细胞,应进行血涂片和流式细胞术检查。除非在过去12个月内已进行,否则还必须进行完整的乙型肝炎(包括核心抗体)、丙型肝炎和人类免疫缺陷病毒的血清学检查。通常不需要正式评估心功能,但对于已知或疑似心脏疾病以及既往有蒽环类药物暴露史的老年患者,应考虑进行评估,因为心功能受损在CRS背景下会带来额外风险。对于心功能受损的患者,应转诊至心脏科或心脏肿瘤服务机构。
建议在开始治疗前进行正电子发射断层扫描/计算机断层扫描(PET-CT),因其可提示肿瘤负荷并为后续反应评估提供基线。高肿瘤负荷预示着CRS风险增加和预后较差。建议对代表性组织进行活检,用于疾病的组织学确认,除非其构成不可接受的风险。虽然在开始 BsAb 治疗前通过免疫组织化学评估 CD20 表达并非必需,临床试验通常不需要证明患者入组的靶抗原,但新出现的数据表明,CD20表达确实与临床缓解相关,免疫组化弱表达或无表达可能与缓解不佳和发生耐药相关。因此,在不存在组织学 CD20 表达的情况下,考虑抗CD3×CD20BsAb时应谨慎。不需要对书写进行常规基线评价或对免疫效应细胞相关脑病 (ICE) 评分进行正式评估,但如果存在认知受损问题,可考虑进行。
实施BSAB治疗的实用考虑
医护人员培训
制定新治疗路径的一个重要方面是对所有参与接受BsAb治疗患者护理的医护人员(HCPs)进行教育和提高认识,包括治疗机构急性入院路径中可能接触到出现BsAb毒性的患者的医护人员。在较小的治疗中心,急诊入院不会直接到血液科或肿瘤科单元,但参与入院路径的HCPs必须了解CRS和ICANS是BsAb治疗可能的副作用,并应知道联系谁以获得紧急建议。虽然让ICU医生参与是有用的,但ICU的使用需求很低,英国RWE中仅有5%的入住率。托珠单抗常用于治疗CRS,血液科病房/急救药柜应常规并随时备有至少两剂(4×400 mg 瓶)的库存。工作人员必须知道托珠单抗在医院内的位置,并随时能够快速获取。药房必须制定补充托珠单抗库存的系统,任何库存问题都应及时通知血液科团队。每个治疗中心最好有一个HCP团队,负责领导对参与管理接受BsAb治疗患者的工作人员进行培训,并为患者和护理人员教育提供信息。
BsAb给药
目前获批的CD3 × CD20 BsAb的比较、其给药方案、剂量延迟管理、重新初始给药和CRS缓解策略见表1。HCPs还应参考每种产品的说明书(summary of product characteristics,SmPC)。不同BsAb的治疗方案之间存在共性,但也有显著差异。Epocritamab是皮下注射,而格菲妥单抗、莫妥珠单抗和odronextamab通过静脉(IV)输注给药。治疗中心必须熟悉这些,并评估其对服务的影响,包括人员资源、药房无菌制剂单元容量、日间单元容量以及任何强制性的住院要求。
鉴于某些BsAb的无菌配制要求较高,早期与医院药房无菌制剂单元沟通至关重要。鉴于 BsAb 的复溶后有效期较短 (24-72 h) 且为某些 BsAb 进行了复杂的无菌制备(例如,连续稀释epcoritamab),建议提前开具全身性抗癌治疗 (systemic anti-cancer treatment,SACT) 处方,以确保有足够的库存和经过培训的药房工作人员来制备BsAb。
CRS和ICANS缓解策略
缓解CRS和ICANS的策略,如SUD和类固醇预用药,已常规纳入BsAb给药方案,并在各自的说明书中有所反映。旨在缩短达到全治疗剂量时间的加速SUD策略正在探索中,并且似乎可以在不增加CRS或ICANS风险的情况下实施。此外,BsAb特异性策略,如epcoritamab的皮下给药和格菲妥单抗前使用奥妥珠单抗预处理以耗竭循环B细胞,旨在降低CRS风险。皮质类固醇预防在SUD期间至关重要,地塞米松在降低CRS发生率和严重程度方面似乎比其他皮质类固醇更有效。根据个别产品指南以及先前是否发生过CRS,类固醇预用药可能需要在后续周期中继续。据报道,给药前给患者补水也是epcoritamab的一种潜在CRS缓解策略。
从治疗开始起,发生CRS的最大风险期因产品而异。目前强制要求在进行周期1 SUD期间(格菲妥单抗为C1 D8,epcoritamab为C1 D15)BsAb给药后选择性住院至少24小时以进行CRS监测。对于odronextamab,ELM-2研究中的患者在SUD期间每次输注后(即C1 D1、C1 D2、C1 D8、C1 D9、C1 D15、C1 D16和C2 D1)均住院监测至少24小时。如果患者住院监测,建议定期(至少每4小时)检查生命体征。在没有CRS的情况下,患者通常可以在给药后24小时出院。鉴于神经毒性不常见,除非有临床担忧或CRS > 2级,否则不需要执行常规ICE和ICANS评估,当CRS > 2级时,应每4小时定期进行ICE评分。鉴于在SUD阶段有显著的类固醇暴露,对于糖尿病或糖尿病前期患者的血糖控制和管理需要加以关注。
患者和护理人员教育及家庭监测
应向患者和护理人员提供有关CRS和ICANS的适当信息、需要注意的症状以及自我监测的建议。图1提供了一个模板,各中心可酌情进行调整。建议指导患者在家每次SUD后48小时内每天监测三次体温,直到一次全剂量给药后未出现CRS。必须向患者提供SACT红色警示卡,上面写明何时呼叫谁以及何时直接前往医院。建议还向患者提供BsAb警示卡或带有血液科团队联系信息的手环。
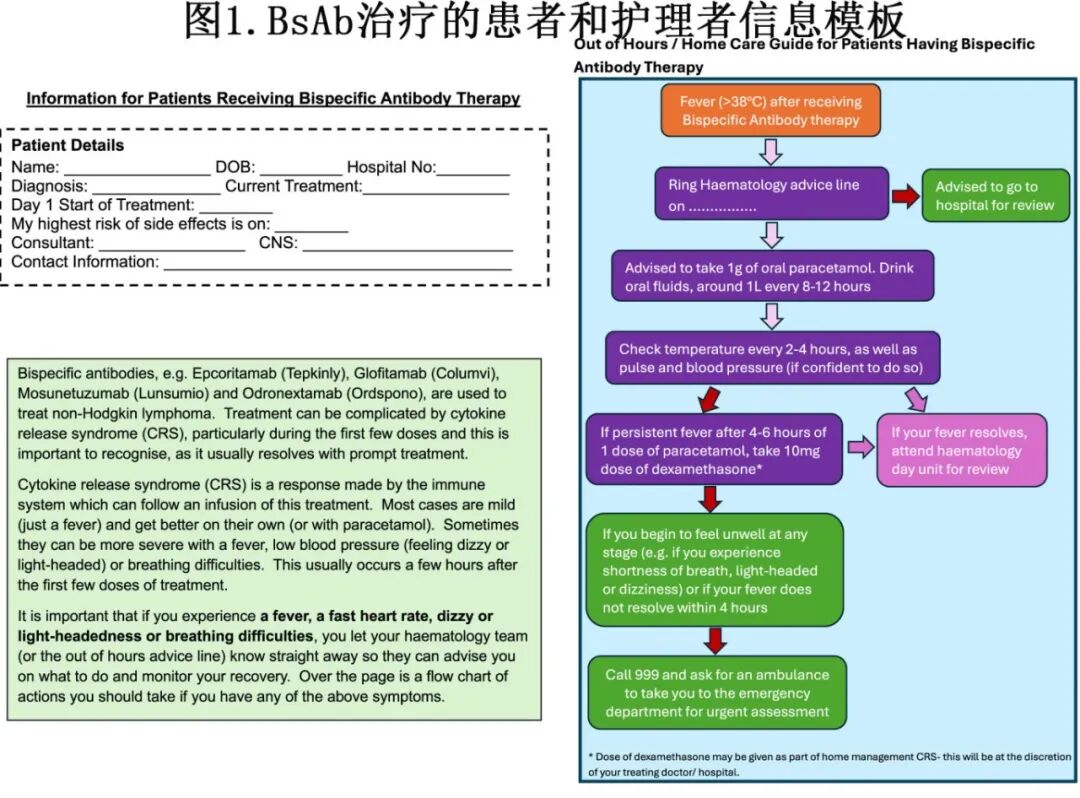
对于特定高危患者,在每次SUD后24和48小时由HCP进行额外的电话随访可能有益。高危患者是指那些具有高肿瘤负荷、器官功能受损(例如肾功能或心功能受损)、老年患者(例如年龄>75岁)以及社会支持有限的患者。对于具有多种风险因素的患者,考虑在每次SUD后24和48小时由HCP进行面对面门诊复查,甚至考虑给药后住院最多48小时。
与CAR-T细胞疗法不同,BsAb治疗后没有强制要求护理人员与患者同住。
识别和管理BSAB相关毒性
CRS、ICANS和其他毒性的频率总结见表2。
CRS分级和管理
CRS是CD3 x CD20 BsAb治疗中由T细胞激活介导的最常见的急性毒性,常发生在周期1 SUD期间,通常为低级别,并且相对于给药时间具有可预测的发生时间。CRS最常见的表现为发热(>38°C)、心动过速、低血压、寒战和低氧血症。输注相关反应(IRR)在临床上可能与CRS表现难以区分。应评估患者发热、低氧血症和低血压的其他原因,例如感染或败血症。CRS和ICANS的分级应使用美国移植与细胞治疗学会(ASTCT)共识标准进行(该分级来自CAR-T)。图2提供了CRS管理的流程图。
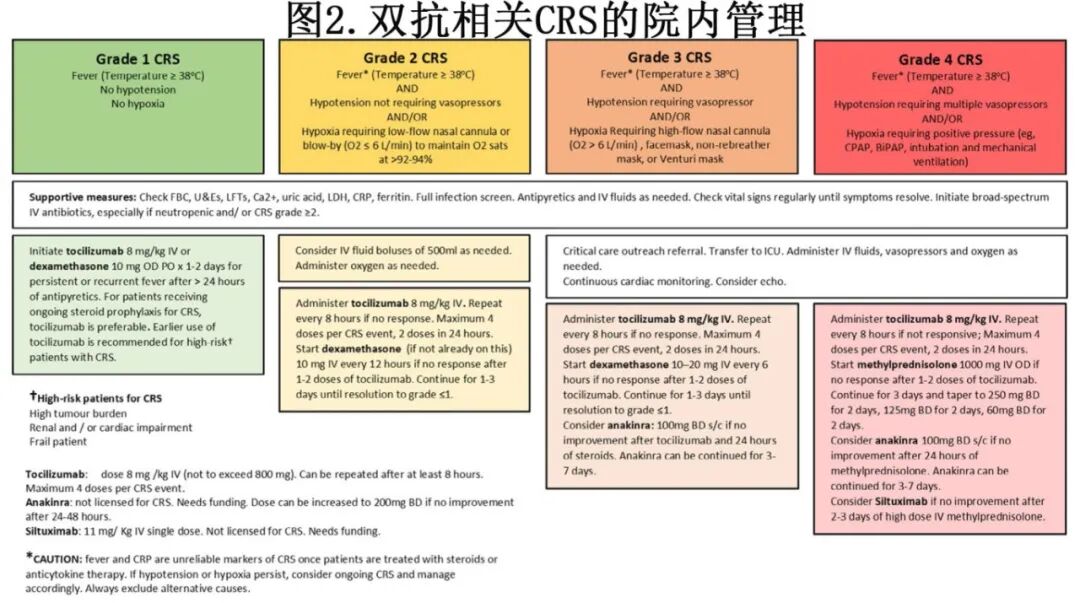
尽管不同产品的说明书对CRS管理的建议存在细微差异,但其原则相似,允许对所有淋巴瘤BsAb采用一致的处理方法。1级CRS通常采用对症治疗措施。持续时间超过24小时的1级CRS应使用托珠单抗或地塞米松治疗。对于在接受类固醇预防治疗期间出现CRS的患者,建议使用托珠单抗。对于肿瘤负荷高的患者,建议早期使用托珠单抗,因为这类患者发生更高级别CRS的风险增加,以及对于那些生理储备减少的患者也是如此,例如心脏或肾功能受损的患者。鉴于CRS和感染在临床上的相似性,建议进行全面的败血症筛查。对于中性粒细胞减少症患者和/或CRS等级≥2的患者,建议开始使用广谱静脉抗生素。对于CRS等级≥2的患者,建议使用托珠单抗。需要注意的是,一旦患者接受抗细胞因子治疗(如托珠单抗),发热和CRP(C反应蛋白)就不再是CRS和感染的可靠标志物。如果低血压或低氧血症持续存在,应考虑持续的CRS并相应地进行管理。须排除临床表现的其他原因。3至4级CRS在接受BsAb治疗时非常罕见,需要入住重症监护病房。对于任何级别的CRS,BsAb治疗应持续直到CRS完全缓解至少72小时。如果下一次给药有延迟,可能需要重新启动(见表1和产品说明书)。对于发生CRS等级≥2的患者,建议在下次剂量时选择性住院进行监测,并继续使用类固醇预防治疗。与接受强化化疗方案后中性粒细胞减少性败血症的风险一样,一些患者也可能因其他原因从选择性再入院中受益;例如,如果患者社交隔离,且担心在家中发生CRS时寻求帮助的能力。
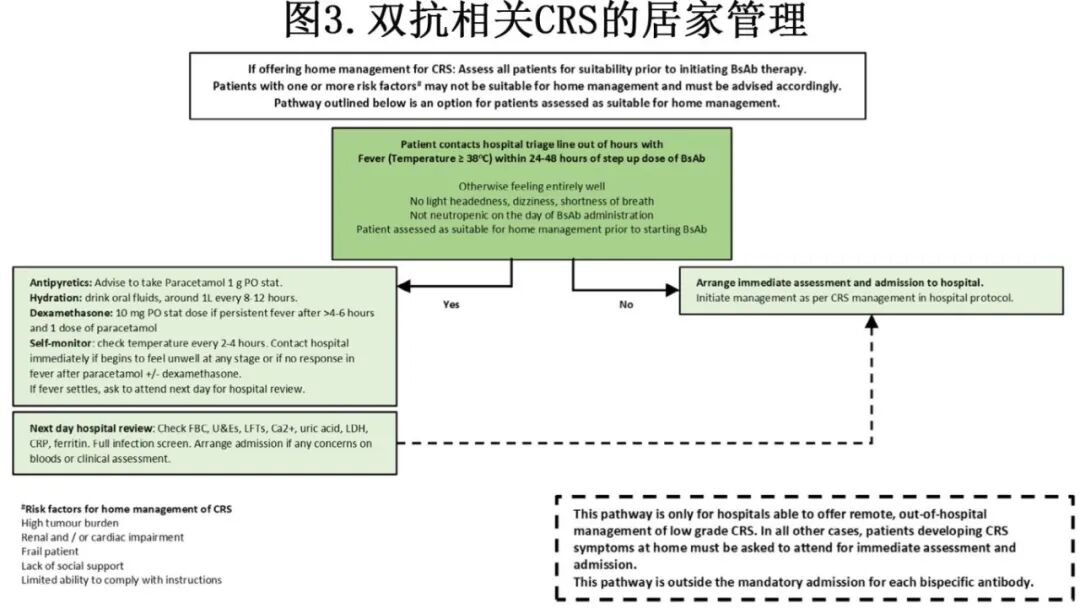
由于在SUD期间CRS风险最高的时间点,大多数BsAb治疗目前都要求在规定的时点进行选择性住院,因此许多CRS事件在住院环境中发生并得到管理。然而,CRS也可能发生在规定的住院时间之外,即患者居家观察。对于这种情况,通常建议患者前往医院进行立即评估。鉴于CRS的可预测性和通常较低的等级,一些机构正在探索为精心挑选的患者提供远程管理路径,以减少急诊入院。这些路径需要严格的患者选择、全面的患者教育以及明确的获取紧急护理的协议。肿瘤负荷高、器官功能障碍、年龄较大、社会支持有限或依从性差的患者可能不适合远程管理途径。图3展示了该路径的潜在算法。提供CRS居家管理路径的医院应考虑为患者提供10毫克剂量的地塞米松,如果他们在服用扑热息痛后发烧持续,可以服用地塞米松。
神经毒性与ICANS:分级与管理
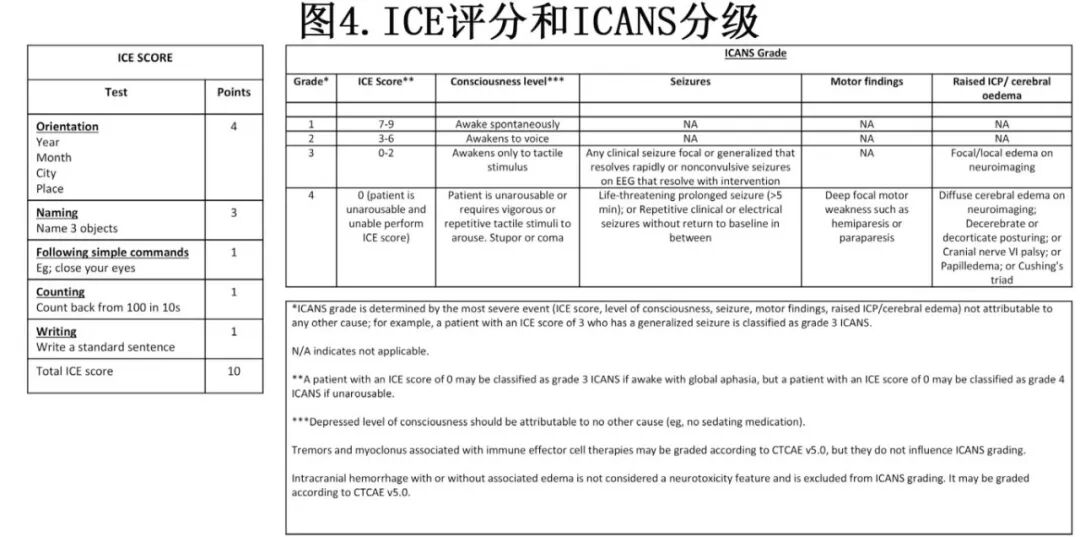
BsAb治疗中观察到的神经毒性最多表现为头痛和头晕。ICANS样神经毒性表现为找词困难、书写障碍或急性意识混乱状态,基本为低级别;更严重的神经毒性较为罕见。ICANS的风险在第1周期最高,但有时也可能出现延迟性发作。如果怀疑ICANS,应进行彻底的神经学检查,包括ICE(免疫效应细胞相关脑病)评估。ICE评分和ICANS分级见图4。
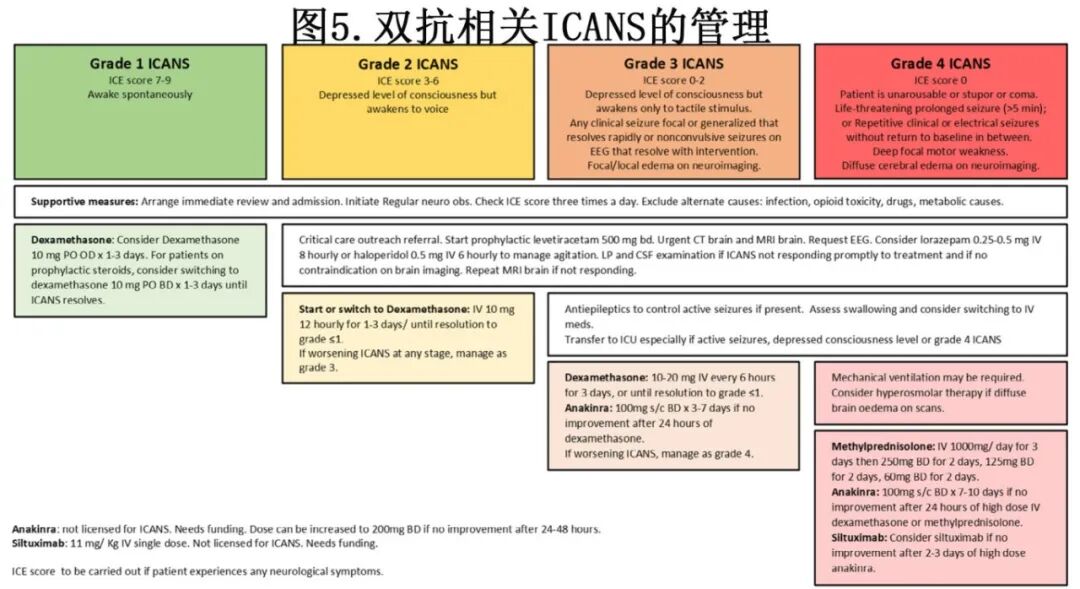
1级ICANS可采用口服地塞米松治疗。2级ICANS需要使用静脉地塞米松和预防性抗癫痫药物(如左乙拉西坦)进行治疗。必须排除其他神经毒性原因,例如感染、阿片类药物毒性、药物和代谢原因。3级和4级较为罕见,应在ICU中进行管理,且需考虑其他病因。3级和4级ICANS的管理应使用静脉地塞米松和阿那白滞素(anakinra),但部分患者可能需要大剂量甲泼尼龙和司妥昔单抗。ICANS分级和管理的推荐算法见图5。
输液相关反应
IRR(输液相关反应)的表现可能与CRS在临床上相同,但通常发生得更早。如果在BsAb输液期间发生IRR/CRS,应中断输液并治疗症状。一旦症状缓解,可以根据BsAb的不同,以相同或更慢的速度重新开始输液,但在4级IRR的情况下可能需要永久停药(具体细节请参考产品说明书)。如果怀疑CRS,应停止输液并遵循CRS管理方案。
肿瘤燃瘤(flare)反应与肿瘤溶解综合征
肿瘤燃瘤反应(Tumour flare reaction,TFR)是BsAb治疗中已有报道,表现为肿瘤大小的暂时性增加,有时伴有疼痛或发热,如果肿瘤靠近重要结构,如大气道或上腔静脉,可能会引起压迫症状。由于新的或恶化的胸腔积液而引起的呼吸困难也有报道。TFR的发生率报告为:epcoritamab为1.6%(均为2级),格菲妥单抗为11.7%(2级占4.8%,3级占2.8%)。大多数TFR事件发生在第1周期,第2周期之后未有报告。因此,在解释BsAb治疗前两个周期的PET扫描时,可能需要考虑TFR的可能性。尚未确定TFR的具体风险因素;然而,对于肿瘤体积大且靠近气道和/或重要器官的患者,建议谨慎。可以给予镇痛药和皮质类固醇来治疗肿瘤燃瘤反应。
BsAb治疗并不会比传统LBCL疗法带来更高的肿瘤溶解综合征(TLS)风险,报告的发生率约为1%至1.5%。大多数TLS事件发生在第1周期,从治疗开始到发作的时间因BsAb而异(格菲妥单抗为2天中位数,epcoritamab为18天,莫妥珠单抗在第2天和第24天)。TLS的预防、监测和治疗由BSH(英国血液学会)的良好实践文件涵盖,应遵循标准的本地/国家方案。
血细胞减少和感染
在关键试验中,报告的≥3级中性粒细胞减少症的发生率在19%到29%之间,通常对粒细胞集落刺激因子(G-CSF)治疗有反应。建议所有4级中性粒细胞减少症(<0.5×10⁹/L)的患者使用G-CSF,并且对于3级中性粒细胞减少症(<1.0×10⁹/L)的患者,尤其是当中性粒细胞减少症持续存在或恶化时,也应考虑使用。给菲妥单抗治疗中发热性中性粒细胞减少症的发生率为2.1%,epcoritamab治疗中为2.4%。由于中性粒细胞减少症而停止治疗的情况较为少见,但如果出现与感染相关≥3级中性粒细胞减少症且对G-CSF治疗无反应,应考虑停止治疗。对于尽管存在中性粒细胞减少症但仍保持良好的患者,继续BsAb治疗并密切监测可能是最佳选择。
在患者中报告的感染情况(不一定与中性粒细胞减少症有关)的发生率为38%到59%,其中≥3级感染的发生率为15%到33%。报告的常见严重感染包括COVID-19(32%)、临床诊断的肺炎(26%)和败血症(12%)。报告的罕见严重机会性感染包括单纯疱疹病毒/水痘带状疱疹病毒再激活、巨细胞病毒和EB病毒,以及严重的流感、弓形虫病、肺孢子菌肺炎(PJP)和真菌性肺炎。在活动性感染存在的情况下,应暂停BsAb治疗。对于无症状的COVID-19患者,在逐例评估风险与收益后,可能适合继续BsAb治疗。建议在整个BsAb治疗期间以及直到CD4计数恢复至>0.2×10⁹/L时,进行水痘带状疱疹病毒(VZV)和PJP预防。通常不需要进行抗真菌预防。对于这些患者,疫苗接种的最佳时机和有效性尚未确定,但应避免使用活疫苗。然而,建议患者接种所有常规的非活疫苗,包括COVID-19、流感和水痘带状疱疹疫苗(如可获得)。
低丙种球蛋白血症和B细胞再生障碍
CD3×CD20BsAb会导致严重且长期的B细胞再生障碍和低丙种球蛋白血症。在接受epcoritamab持续治疗的患者中,血清IgG水平平均下降约20%,并且随着时间的推移保持稳定。在接受固定疗程的格菲妥单抗治疗后,从治疗结束大约18个月开始观察到B细胞再生障碍和IgG水平的恢复。持续的IgG水平<4g/L与更高的感染风险相关。对于接受了抗菌预防但仍然出现反复或严重感染且IgG水平<4g/L的患者,应考虑进行免疫球蛋白替代疗法(IGRT)。对于在CAR-T细胞治疗后开始BsAb治疗以治疗进展性疾病(PD)的患者,可能会出现更严重的B细胞再生障碍和低丙种球蛋白血症,尽管需要来自真实世界研究的进一步数据来支持这一点。
如果患者处于持久缓解状态,持续治疗方案中的一些患者可能会面临慢性低级别不良反应的挑战,例如感染和治疗疲劳。对于处于持续完全缓解(CR)状态的患者,在继续治疗的获益被累积毒性所抵消的情况下,考虑停止治疗可能是合理的。目前可用的数据表明,即使在停止epcoritamab治疗后,一部分患者的CR仍可持久。
疗效评估
在关键临床试验中,治疗开始后的6周和12周进行反应评估扫描,大多数缓解发生在这个时间框架内。在日常临床实践中,一个实用的方法是在第3个周期后进行PET-CT扫描,除非有临床对疾病进展的担忧,但也应认识到许多患者不会产生反应。重要的是不要过早地在PET扫描上得出稳定疾病或PD反应的结论,特别是在BsAb治疗开始后不久进行的PET扫描。BsAb治疗报告了肿瘤燃瘤反应,通常发生在治疗早期,应与真正的进展区分开来。如果患者在临床上仍然良好,通常更倾向于继续治疗,并在停止治疗前重新扫描或进行活检。
对于在三个周期后达到完全代谢缓解(CMR)的患者,可以在第12个周期后考虑进行重复PET扫描,以记录持续的反应状态。对于在三个周期后没有达到CMR的患者,建议在另外三个周期后进行进一步的PET-CT扫描,并根据临床情况继续进行。
相关建议
•患者是否适合 BsAb 治疗的基线评估必须包括体能状态和器官功能评估。(1A)
•在开始 BsAb 治疗前进行基线 PET-CT 扫描,以评估肿瘤负荷。(1B)
•建议对代表性组织进行活检以确认组织学,除非临床上不安全。(1B)
•参与 BsAb 治疗患者急诊入院途径的 HCP 应知道联系谁寻求建议,需要随时获得该建议。(1C)
•血液科病房/急救药物橱柜中应至少有两种剂量(4 × 400 mg小瓶)的托珠单抗库存。(1B)
•CRS应根据 ASTCT 标准进行分级,并根据图2中概述的严重程度分级进行管理。(1B)
•对于肿瘤负荷高和/或生理储备降低的1级 CRS 患者,在早期给予托珠单抗。(1B)
•对所有疑似 CRS 患者进行感染筛查。(1B)
•对于任何级别 CRS 的中性粒细胞减少症患者和/或CRS≥2级的患者,开始广谱 IV 抗生素治疗。(1B)
•ICANS应根据 ASTCT 标准进行分级,并根据图5中概述的严重程度分级进行管理。(1B)
•必须中断 BsAb 治疗,直至 CRS 或 ICANS 消退。根据给药中断的持续时间,可能需要重复SUD。(1B)
•存在严重、活动性感染时中断 BsAb 治疗。(1B)
•尽管进行了抗生素预防,IgG水平<4 g/L,但复发性重度或长期感染患者仍考虑IGRT。(2B)
•建议在整个 BsAb 治疗期间预防 VZV 和PJP,直至 CD4 计数恢复至>0.2 × 109/L。(1B)
•提供包括 COVID-19 在内的常规非活疫苗接种流感和水痘带状疱疹,但接受 BsAb 治疗的患者应避免接种活疫苗。(1C)
参考文献
Chaganti S, Dulobdas V, Wilson MR, Tucker D, Townsend W, Parry-Jones N, et al. Clinical management of bispecific antibody therapy for lymphoma: A British Society for Haematology Good Practice Paper. Br J Haematol. 2025;00:1–15. https://doi.org/10.1111/bjh.70018


