新研究揭秘肿瘤微环境中的“隐形战士”,肿瘤浸润B细胞在结直肠癌中的关键作用
时间:2025-09-15 12:12:56 热度:37.1℃ 作者:网络
近年来,随着肿瘤免疫学的快速发展,肿瘤微环境(TME)中的免疫细胞角色愈发受到关注。众所周知,肿瘤浸润T细胞(TILs)在结直肠癌(CRC)中的密度与患者预后密切相关,成为预后判定和治疗决策的重要指标。结直肠癌作为全球第三大常见恶性肿瘤,其发病率和死亡率居高不下。肿瘤微环境由肿瘤细胞、免疫细胞、基质细胞及细胞因子等组成,免疫细胞的组成及功能状态直接影响肿瘤的进展和患者生存。
除了T细胞,B细胞在抗体产生、抗原呈递和免疫调节等方面扮演多重角色,越来越多的证据表明B细胞亚群的动态变化与肿瘤免疫逃逸和免疫治疗反应密切相关。然而,相较于T细胞,肿瘤浸润B细胞(TIBLs)的研究起步较晚,系统性的综述较为缺乏。本文基于最新的系统回顾,聚焦于结直肠癌TME中B细胞的多种亚群、识别方法及其临床预后价值,探讨其潜在的免疫调节机制和治疗前景。

本次综述采纳了2000年至2025年间发表的相关文献,通过PubMed、Embase和Cochrane Library数据库进行系统检索,严格按照PRISMA指南筛选符合条件的研究。最终纳入32篇原创文章,涵盖5766名个体患者的临床数据和组织学分析,确保了数据的广泛性和代表性。各研究中采用的B细胞识别手段包括免疫组化(IHC)、流式细胞术、多重免疫荧光及基因表达谱分析等,方法多样性反映了领域内研究技术的进步和挑战。
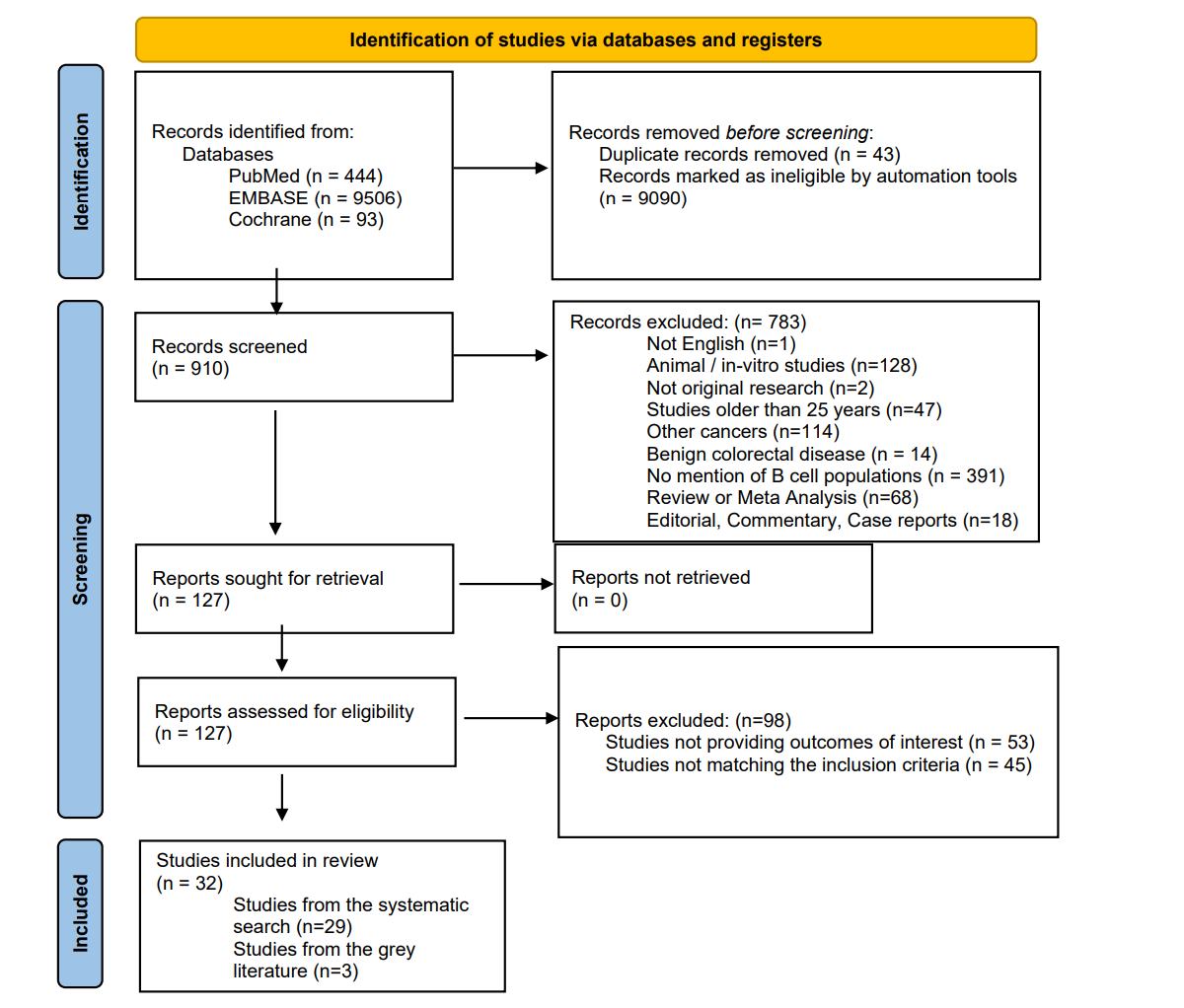
图:研究流程图
结果发现,结直肠癌肿瘤微环境中存在多种B细胞亚群,包括但不限于记忆B细胞、浆细胞、调节性B细胞(Bregs)和抗原呈递B细胞等。各亚群在免疫应答中扮演不同角色:
记忆B细胞:增强特异性抗肿瘤免疫反应,促进长期免疫监控。
浆细胞:产生抗体,参与肿瘤相关抗原的识别和清除。
调节性B细胞(Bregs):通过分泌免疫抑制因子如IL-10调节免疫反应,可能促进肿瘤免疫逃逸。
抗原呈递B细胞:作为抗原呈递细胞与T细胞交互,参与免疫激活。
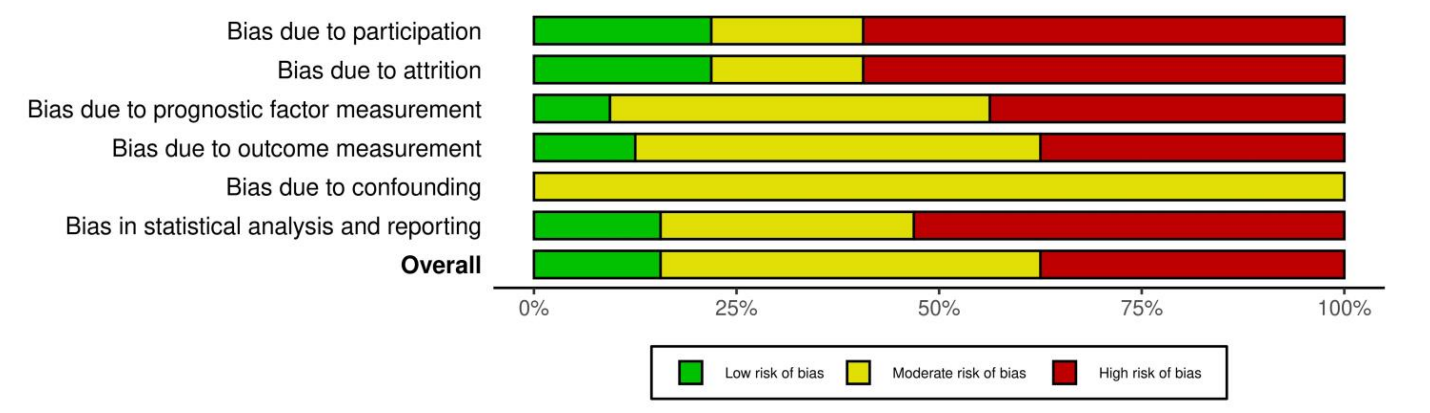
图:偏倚风险评估总结
这些B细胞亚群的分布及比例在不同临床分期和病理类型中存在差异,且与患者的生存率和复发风险密切相关。部分研究显示,高密度的某些B细胞亚群预示着良好的预后,而某些免疫抑制性B细胞则可能与不良预后相关。
多种方法被用于识别和定量TIBLs:
免疫组化(IHC):通过标记CD20、CD19等B细胞表面标志,直观评估细胞密度。
流式细胞术:细分B细胞亚群,揭示功能状态。
多重免疫荧光:实现多标记同时检测,揭示细胞间空间关系。
基因表达谱和单细胞测序:深入分析B细胞的转录组特征和功能多样性。
这些技术的结合使用有助于全面了解B细胞在肿瘤中的动态变化和功能状态,为精准免疫治疗提供技术保障。
研究还探讨了TIBLs参与肿瘤发生发展的免疫途径,如B细胞介导的抗体依赖性细胞毒性反应、免疫调节因子分泌影响T细胞活性等。调节性B细胞通过IL-10等分子抑制效应性T细胞,促进肿瘤免疫逃逸。了解这些机制不仅揭示了肿瘤免疫逃逸的复杂网络,也为开发新型免疫治疗策略提供了理论基础,如靶向Bregs的抑制剂或增强抗肿瘤B细胞功能的免疫激活剂。
综上,肿瘤浸润B细胞是结直肠癌免疫微环境的重要组成部分,不同亚群的存在与肿瘤进展和患者预后密切相关。深入理解其功能和作用机制有望成为精准免疫治疗的突破口,助力个体化治疗方案的制定。未来的研究需聚焦于B细胞亚群的动态变化、空间分布及其与其他免疫细胞的交互作用,同时推动相关检测技术标准化,提升临床应用价值。
原始出处
Fagarasan, G.; Fagarasan, V.; Bintintan, V.V.; Dindelegan, G.C. The Role of Tumor-Infiltrating B Lymphocytes in Colorectal Cancer Patients: A Systematic Review of Immune Landscape Evolution. Cancers 2025, 17, 2996. https://doi.org/10.3390/cancers17182996
本文相关学术信息由梅斯医学提供,基于自主研发的人工智能学术机器人完成翻译后邀请临床医师进行再次校对。如有内容上的不准确请留言给我们。


