呼出气体挥发性有机化合物对肺囊性纤维化诊断价值的系统评价
时间:2025-09-18 12:12:39 热度:37.1℃ 作者:网络
摘 要
目的 探讨呼出气体挥发性有机化合物(volatile organic compounds,VOCs)对囊性纤维化(cystic fibrosis,CF)的诊断价值。方法 系统检索PubMed、EMbase、Web of Science、Cochrane Library、中国知网、万方、维普以及中国生物医学文献数据库,检索时限为建库至2024年8月7日。对符合纳入标准的研究进行数据提取和质量评估。采用纽卡斯尔-渥太华量表(Newcastle-Ottawa Scale,NOS)对纳入研究进行质量评价,采用预测模型偏倚风险评估工具(prediction model risk of bias assessment tool,PROBAST)对纳入预测模型研究的偏倚风险和适用性进行评估。结果 共纳入10项研究,NOS评分为7~10分。其中5项研究仅识别CF患者特异性呼出气体VOCs,另外5项在识别VOCs的基础上开发了7个CF风险预测模型。纳入研究共报道75个呼出气体VOCs,这些化合物多属于酰基肉毒碱类、醛类、酸类和酯类。大多数模型(n=6,85.7%)仅纳入呼出气体VOCs作为预测因子,只有1个模型纳入VOCs以外的因素,包括用力呼出75%肺活量时的瞬间呼气流量和呼吸困难分级量表评分。模型的准确度为77%~100%,受试者工作特征曲线下面积范围为0.771~0.988,纳入研究均未提供模型的校准度信息。PROBAST结果显示,所有预测模型研究的总体偏倚风险高,总体适用性不清楚。结论 纳入研究的呼出气体VOCs具有显著异质性,后续需开展更多研究探索CF特异性化合物。此外,基于呼出气体VOCs的风险预测模型在诊断CF方面有一定价值,但整体偏倚风险较高,需从模型构建及验证等方面进一步优化。
正 文
囊性纤维化(cystic fibrosis,CF)是一种常染色体隐性遗传病,由囊性纤维化跨膜传导调节因子(cystic fibrosis transmembrane conductance regulator,CFTR)基因突变引起,常累及多个系统[1]。呼吸系统功能减退和肺部疾病恶化是CF患者重要的临床症状[2-4]。CF患者呼吸道黏膜纤毛的清除和防御机制受损,易被机会致病菌定植、感染,进而引起慢性炎症、支气管阻塞、呼吸衰竭,甚至死亡[5]。CF在高加索人群中相对常见,发病率为1/4 000~1/3 000[6]。目前我国报道的CF数量仅为200例[7],而近10年CF患者数量超过了既往30年总和的2.5倍[8],这表明我国CF的发病率可能被严重低估。诊断CF通常依据临床症状和体征,如果症状不典型,则进行汗液氯离子测定和/或基因分析[7]。然而,利用现有技术诊断CF存在汗液样本采集不足、基因检测费用高等问题[9]。因此,亟需开发一种新的辅助诊断技术,以提高对可疑患者的诊断准确性。
呼出气体是一种丰富的介质,由气相有机化合物、气相无机化合物、水蒸气和气溶胶组成。其中,气相有机化合物中包含了数千种以微量形式存在的挥发性有机化合物(volatile organic compounds,VOCs)[10]。大多数VOCs都参与了人体组织水平的内源性代谢过程。当出现病理状况时,VOCs的种类和含量则通过体内氧化应激、细胞色素p-450和脂质代谢等途径发生变化[11]。既往研究[12-13]发现,CF患者呼出气体正戊烷、乙酸等化合物浓度高于对照组,而二甲基硫和1,2,4,5-四甲苯等化合物浓度较对照组显著降低[14-15]。这些研究提示呼出气体VOCs很可能作为CF的潜在生物标志物。相较于传统的实验室检查或基因检测,分析呼出气体VOCs具有无创、操作简捷等优点[16],有望成为辅助诊断CF的新方法。
近年来,全球开展了多项基于呼出气体VOCs诊断CF的研究[12-15, 17-22],但研究结论尚有争议。因此,本系统评价旨在全面分析呼出气体VOCs对CF的诊断价值。
1 资料与方法
1.1 文献纳入和排除标准
纳入标准:(1)研究对象为CF患者;(2)研究内容为识别CF患者特异性呼出气体VOCs或构建基于呼出气体VOCs的CF风险预测模型;(3)研究类型为队列研究、病例对照研究和横断面研究等;(4)发表语言为中文或英文。排除标准:(1)VOCs来源于呼出气体冷凝物或血液、尿液等其他生物样本;(2)外源性VOCs;(3)摘要、综述、会议论文等;(4)重复发表的文献。
1.2 文献检索策略
计算机检索PubMed、EMbase、Web of Science、Cochrane Library、中国知网、万方、维普以及中国生物医学文献数据库,搜集国内外公开发表的基于呼出气体VOCs诊断CF的研究,并追溯纳入研究的参考文献。检索时限为建库至2024年8月7日。采用医学主题词与自由词结合的方式进行文献检索。中文数据库以中国知网为例,检索式为:(主题“囊性纤维化”OR主题“肺囊性纤维化”OR主题“肺部囊性纤维化”)AND(主题“呼出气体”OR主题“呼出气体检测”OR主题“呼出气体分析”)AND(主题“挥发性有机化合物”OR主题“挥发性有机气体”)。英文数据库以PubMed为例,检索式为:(((cystic fibrosis[MeSH Terms]) OR (fibrosis, cystic or mucoviscidosis or pulmonary cystic fibrosis or cystic fibrosis, pulmonary)) AND ((volatile organic compounds[MeSH Terms]) OR (compounds, volatile organic or organic compounds, volatile or volatile organic compound or compound, volatile organic or organic compound, volatile))) AND ((exhaled) OR (breath))。
1.3 文献筛选与资料提取
剔除重复文献后,由2名研究人员独立完成文献筛选与资料提取,并交叉核对。运用EndNote 20软件剔除重复文献,阅读文章题目与摘要进行文献初筛,再阅读全文进行二次筛选,剔除不符合要求的文献后,确定最终纳入文献。若存在意见分歧,则与第3名研究者讨论解决。提取并归纳文献资料:(1)文献基本信息,包括第一作者、发表年份、国家、研究类型、样本量等;(2)呼出气体VOCs的识别情况;(3)基于VOCs的CF风险预测模型的构建及预测性能,包括候选变量、纳入变量、模型构建及验证方法、模型性能等。
1.4 文献质量评价
采用纽卡斯尔-渥太华量表(Newcastle-Ottawa Scale,NOS)对纳入研究进行质量评价[23-24],包括研究人群的选择、组间可比性、暴露因素或结果测量3个方面。病例对照研究的NOS总分为9分,横断面研究的NOS总分为10分。评分≤4分为低质量,5~6分为中等质量,≥7分为高质量。
使用预测模型偏倚风险评估工具(prediction model risk of bias assessment tool,PROBAST)对纳入预测模型研究的偏倚风险和适用性进行评估[25-26]。偏倚风险包括研究对象、预测因子、结果和统计分析4个领域,适用性包括研究对象、预测因子和结果3个领域。若2名研究者在质量评价过程中存在意见分歧,则与第3名研究者讨论解决。
2 结果
2.1 文献筛选流程及结果
初步检索得到文献373篇,均为英文文献。去重后剩余文献195篇,阅读题目与摘要后排除177篇,继续阅读全文后排除8篇,最终纳入10篇文献[12-15,17-22]。文献筛选流程见图1。
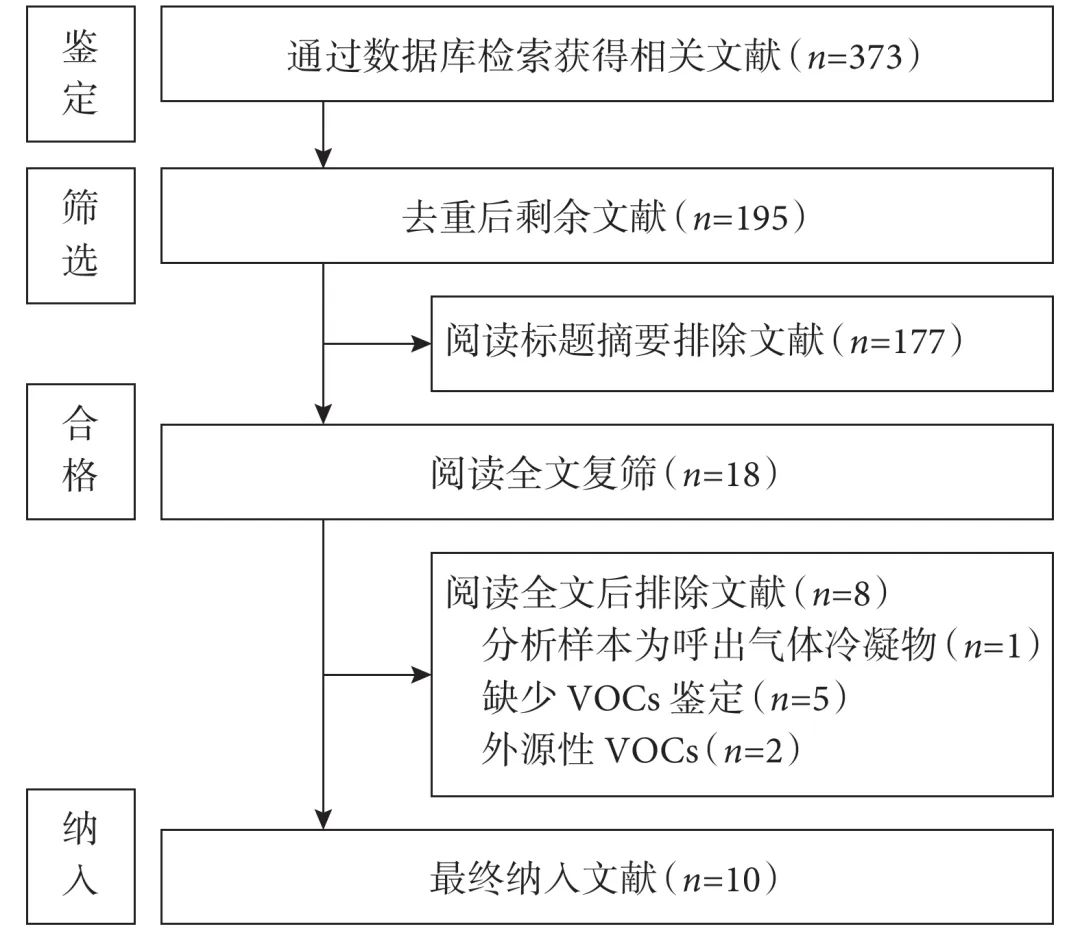
图1 文献筛选流程图
VOCs:挥发性有机化合物
2.2 纳入研究的基本特征
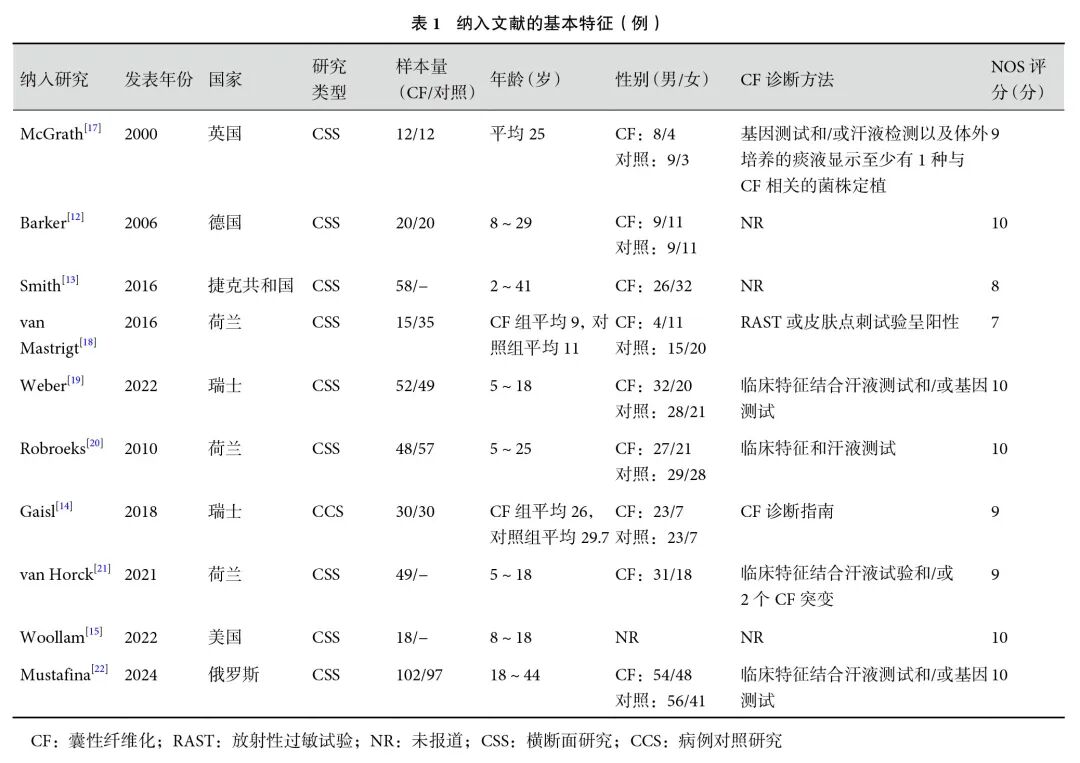
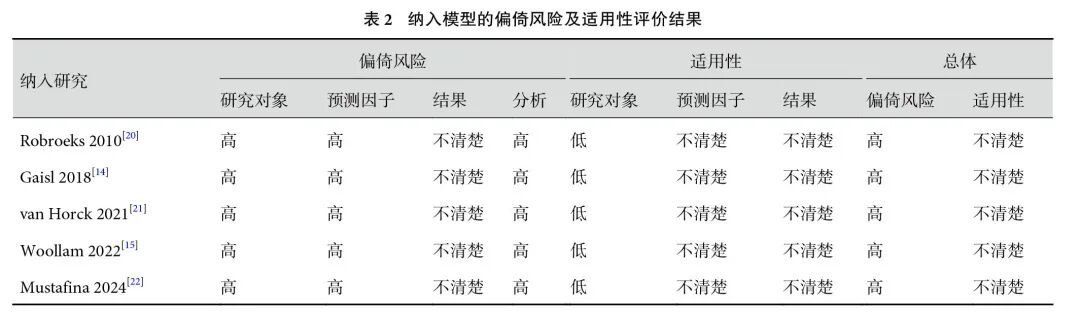
纳入的10项研究共包括404例CF患者和300例健康对照者。其中9项(90%)研究采用横断面研究设计,1项(10%)为病例对照研究。8项(80%)研究发表于近10年。纳入研究的人群数据来自欧洲(n=9,90%)和北美洲(n=1,10%)。纳入研究的NOS评分为7~10分,均为高质量文献。纳入文献的基本特征见表1。PROBAST结果显示,所有预测模型研究(n=5)总体偏倚风险为高偏倚风险,总体适用性不清楚。在模型的偏倚风险方面,所有研究在研究对象、预测因子和统计分析领域被评为高风险,在结果领域的偏倚风险未知。关于模型的适用性,所有研究在研究对象领域有较低的适用性风险,在预测因子和结果领域的风险未知;见表2。
2.3 呼出气体VOCs的识别
纳入的10项研究共识别75个呼出气体VOCs,这些化合物多属于酰基肉毒碱类、醛类、酸类和酯类。所有VOCs均仅被报告了一次。6项研究分析报道了CF患者与健康受试者呼出气体VOCs的浓度差异。与CF相关的呼出气体VOCs见附表1。
2.4 基于VOCs的CF风险预测模型的构建情况
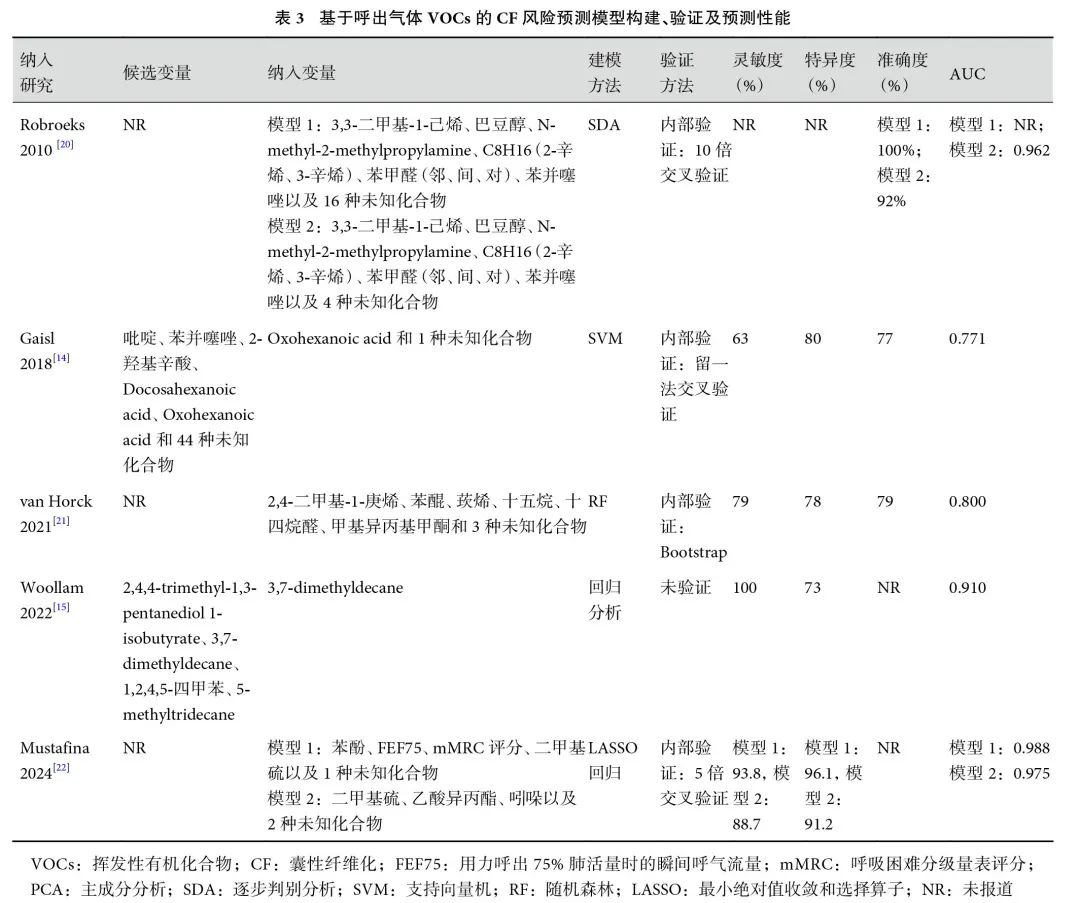
5项预测模型研究[14-15,20-22]共构建7个基于呼出气体VOCs的CF风险预测模型。样本总量为18~199例,CF患者12~97例。仅有1个基于呼出气体VOCs的模型纳入了用力呼出75%肺活量时的瞬间呼气流量和呼吸困难分级量表评分作为预测因子,其余模型纳入的预测因子均为呼出气体VOCs,纳入模型频数最多的化合物有:3,3-二甲基-1-己烯(n=2)、巴豆醇(n=2)、N-methyl-2-methylpropylamine(n=2)、苯甲醛(n=2)和苯并噻唑(n=2)。纳入研究均采用机器学习算法构建模型。模型的构建情况和性能见表3。
2.5 模型预测性能
模型的区分度主要通过受试者工作特征曲线下面积(area under the curve,AUC)表示。6个模型报道了AUC值,范围为0.771~0.988。所有研究均未提供模型的校准度信息。另外,5个模型报道了灵敏度和特异度指标,其中,灵敏度最高(100%)的模型,其特异度为73%;特异度最高(96.1%)的模型,其灵敏度为93.8%。4个预测模型报道了准确度,范围为77%~100%。
2.6 模型验证
4项研究基于模型开发队列数据进行了内部验证,包括K倍交叉验证(n=2,50%)、留一法交叉验证(n=1,25%)和计算机模拟重复采样法(Bootstrap)(n=1,25%)。另外1项研究未对模型进行验证。
3 讨论
本系统评价纳入的10项研究中,5项研究[12-13,17-19]仅报道了CF患者特异性呼出气体VOCs,另外5项研究[14-15,20-22]在识别CF特异性呼出气体VOCs的基础上,开发了7个CF风险预测模型。通过对纳入文献报道的呼出气体化合物及模型的构建方法、预测性能、内外部验证情况等的比较,发现纳入研究报道的VOCs存在显著异质性,这些化合物多属于酰基肉毒碱类、醛类、酸类和酯类。此外,基于呼出气体VOCs的CF风险预测模型整体性能较好,但在模型开发和验证过程中存在一些不足,需要对模型进一步优化。
本研究纳入模型的预测因子多为呼出气体VOCs,缺乏其他重要因素。既往研究[27-28]发现巨噬细胞、中性粒细胞、淋巴细胞等炎症细胞以及8-异前列腺素和白细胞介素8等炎症介质在CF发病机制中发挥了重要作用,提示机体炎性介质是预测CF的重要因素。此外,研究发现某些具有先天防御功能的蛋白质(如分泌型白细胞蛋白酶抑制剂、脂质运载蛋白-1和胱抑素SA),其丰度在肺部疾病频繁加重的CF患者的痰液中升高[29],提示可寻找适用于临床实践的痰液标志物作为CF的预测因子。
本研究纳入文献均基于欧美人群开展,一方面可能是因为携带CFTR突变基因的高加索人群数量较大[30],另一方面可能是因为这些地区的人们对CF的重视程度高,国家资金投入大,诊断治疗技术处于国际领先水平,有利于CF的检出[31]。建议今后在构建CF风险预测模型时,综合考虑呼出气体VOCs、实验室指标、体液标志物以及包括种族在内的人口学特征等多方面因素,以提高模型的准确性和临床实用性。
本研究纳入的CF风险预测模型具有良好的预测性能,但模型在开发和验证过程中存在一些方法学缺陷,导致纳入研究的偏倚风险普遍偏高。在数据来源方面,5项研究为单中心回顾性研究。虽然回顾性数据易获取,但在构建模型时易产生回忆偏倚,且无法获得预测因子和研究结局之间的因果关系。PROBAST推荐采用队列研究或巢式病例对照研究等前瞻性数据以减少此类偏倚[25-26]。在样本量方面,2项研究的每个自变量的事件数(events per variable,EPV)<10,导致建模过程可能出现过度拟合[32]。研究[33]表明,当模型开发研究的EPV≥20时,模型的回归系数通常能较好地代表真实的回归系数,构建的回归模型准确性也较高。因此,为使模型更加准确,有必要选取大样本量数据构建预测模型[25-26]。在筛选预测因子方面,4项研究采用单因素分析方法。在候选变量较多的情况下,一些变量间可能具有相关性,使用单因素分析可能会丢失重要变量[34]。相比之下,逐步回归、LASSO回归等多变量分析方法可避免多重共线性,同时能进行参数估计和变量选择[35],在预测因子的筛选中应用逐渐广泛[36]。今后构建CF风险预测模型时,可根据实际应用情况选择合适的方法来筛选潜在的预测因子。此外,还应充分考虑临床意义等非统计学方法以降低模型的偏倚风险[34]。最后,在模型性能评估方面,全面报道区分度(如AUC值、C指数)和校准度(如Hosmer-Lemeshow检验、Brier得分等)指标才能明确模型的预测效能[25-26],而纳入研究均未提供校准度信息,使模型性能的评价不够完整,在一定程度上限制了其临床应用。值得注意的是,基于呼出气体VOCs的CF风险预测模型目前尚处于开发阶段,缺少模型验证过程。预测模型的内部验证用于检验模型开发过程的可重复性,防止过度拟合[37],而外部验证关注模型的应用和推广[38]。因此,为确保模型的临床实用性,今后在考虑CF模型预测性能的同时,可以更多地关注模型的验证和完善,以构建性能更好、外推性高的预测模型[39]。
酰基肉毒碱类、醛类、酸类和酯类是纳入研究中报道频率最高的化合物。然而,由于所有VOCs仅报道了1次,使研究间的比较非常复杂。实际上,要完全识别呼出气体中数以千计的VOCs几乎是不可能的[40],因为气体样本在采集和分析过程受很多因素的影响,如环境中的挥发性物质[41]、气体采样袋及分析仪器的本底污染物以及样本存放时间等[42]都会影响检测结果,且基于呼出气体VOCs辅助诊断CF的研究尚处于起步阶段。需开展更多研究进一步探索呼出气体化合物与CF之间的关系。
本系统评价存在一些局限性。首先,本研究仅纳入分析了英文文献,可能导致选择偏倚。其次,由于纳入研究报道的呼出气体VOCs、模型构建方法及预测性能等存在较大异质性,因此未能进行定量分析。最后,绝大多数纳入研究属于横断面研究,不能明确预测因子和结局之间的因果关系。
综上所述,尽管各研究报道的呼出气体VOCs有很大异质性,但基于这类气体标志物的预测模型在辅助诊断CF方面具有一定价值,模型整体偏倚风险较高,需从模型构建及验证等方面进一步优化,为临床医务工作者早期识别CF提供可靠、科学的工具。
利益冲突:无。
作者贡献:龚卫娟、卢光玉提出研究思路,设计研究方案;於晓平、苏志霞、严凯、沙泰宁、何宇航、张艳艳、陶玉坚、郭虹负责数据收集、清洗和统计学分析,绘制图表等;於晓平、苏志霞、卢光玉负责论文起草;龚卫娟负责最终版本修订。
本文附件表1见本刊网站电子版(
https://www.tcsurg.org/article/10.7507/1007-4848.202406075)。


