肝硬化逆转,还是一场文字游戏?
时间:2025-09-12 12:10:34 热度:37.1℃ 作者:网络
一、肝硬化基本病程
肝硬化是一个长期慢性刺激、损伤、修复的病理过程,大致分为如下步骤:
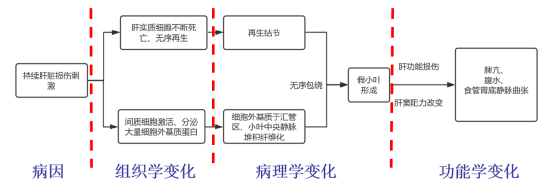
1. 肝硬化始于持续的肝脏损伤刺激,包括但不限于肝炎、代谢、免疫、药物等因素(病因);
2. 肝实质细胞不断死亡、再生,间质细胞激活、分泌大量细胞外基质蛋白、形成纤维化组织(组织学改变);
3. 异常再生的肝细胞形成无规则的“再生结节”,细胞外基质于汇管区、小叶中央静脉不断堆积纤维化,无序包绕再生结节及残留肝小叶,使正常的肝小叶结构紊乱、形成“假小叶”(病理学改变);
4. 最终出现脾亢、食管胃底静脉曲张、腹水等肝硬化失代偿并发症(功能学改变,肝硬化失代偿)。
二、肝硬化逆转研究进展
肝硬化能否逆转,是肝病患者永恒的话题。在以前,肝硬化被认为是不可逆转的临床终末疾病,然而近期出现了大量的研究和观点,论证了肝硬化可逆转,整理如下:
1 长期抗病毒治疗助力抗肝纤维化:
一项纳入179例HBV患者长期抗病毒治疗的研究显示,对基线、治疗1.5年和5年的患者进行连续3次肝穿刺,结果表明,所有患者1.5年的肝纤维化逆转率(Ishak评分下降1级以上)为56.2%,5年逆转率为66.9%。
2 抗脂肪肝治疗助力抗肝纤维化:
Resmetirom是一种靶向肝脏的甲状腺激素受体-β选择性激动剂,通过促进肝脏脂质代谢治疗NASH。2023年初,其纳入966例NASH肝纤维化患者的III期随机双盲临床试验结果公布,用药52周后,80mg组与100mg组肝纤维化改善≥1期且NAS未恶化患者比例分别为24%、26%,而安慰剂组为14%,差异具有统计学意义。
3 生活方式改善有助抗肝纤维化:
部分研究表明,非酒精性脂肪性肝病(NAFLD)患者经过52周的生活方式改善,25%的NASH患者有组织学改善,19%有纤维化逆转;其他疾病如酒精性肝病患者停止饮酒后也会发生组织学纤维化逆转甚至生存率改善;一些体重指数过高的患者中,采用外科减重手术一年后,34%的患者有纤维化逆转。
4 接受病因治疗后门脉高压逆转:
既往研究中,常以HVPG为标准量化评价门脉高压逆转,对于代偿期肝硬化患者HVPG(5-10mmHg)下降≥10%,失代偿期肝硬化患者HVPG(≥16-20 mmHg)下降≥20%或<12mmHg是门脉高压逆转的评价标准之一。
一项纳入11个研究的荟萃分析中,569例患者中的324例HVPG下降≥10%,响应率为56%。另一项包含9个HCV研究、1个NAFLD及1个ALD的荟萃分析中,HVPG下降≥20%作为逆转标准,492例患者中有194例达到了响应值,响应率39%。
5 病因治疗后的肝硬化再代偿:
Baveno VII中对“再代偿”的定义是:
(1)消除/抑制/治愈肝硬化的主要病因(HCV的病毒消除,HBV的SVR,酒精性肝硬化的持续戒酒);
(2)腹水(停用利尿剂)、脑病(停用乳果糖/利福昔明)的缓解和静脉曲张出血复发(至少12个月)的消失;
(3)肝功能检查(白蛋白、INR、胆红素)稳定改善。
国内8家医院联合开展了首次失代偿事件发生后、启动抗病毒治疗的失代偿期乙肝肝硬化患者再代偿发生率的多中心、回顾性研究,结果显示,患者1年、2年、3年再代偿发生率分别为79%,60.5%,45.3%。
6 直接抗纤维化治疗:
纤维化由ECM过度积累引起,主要成分为胶原蛋白,而激活的肝星状细胞和肌成纤维细胞是纤维化的主要效应细胞。通过靶向抑制胶原蛋白合成、交联和整合素等,可以逆转早期肝纤维化。
目前处于临床试验阶段的抗肝纤维化药物包括CC趋化因子受体2/5拮抗剂、法尼醇X受体激动剂、细胞凋亡信号调节激酶(ASK1)抑制剂等,这些药物的作用机制和研究进展正在被积极探讨和总结,以期在肝纤维化的治疗上取得突破。
7 中医药治疗:
一项十三五科技重大专项研究,对比恩替卡韦与联合使用安络化纤治疗HBV肝纤维化的病理改善率。结果显示,基线F3-4患者(217例)在治疗78周后,ETV+ALHX联合组(49.01%)比ETV单药组(31.82%)显著提高17.19%,P=0.020。
78周肝组织学F5降至F1的病例数:安络化纤联合组出现1名F0的患者和17名F1的患者,ETV单药组出现3名F1的患者,联合组(9%)降至F0-1的比例约为单药组(3%)的3倍。机制研究显示,安络化纤能显著抑制TGFβ1生成及相应Smads信号通路的影响,从而抑制肝星状细胞(HSC)激活而发挥抗纤维化作用。其他药物如扶正化瘀胶囊、复方鳖甲软肝片在临床中也广泛应用于抗纤维化。
三、编者观点
据朴素的认知来看,结构紊乱的“假小叶”属于一种从有序走向无序的“熵增”现象,正如“覆水难收”。但为什么众多研究纷纷得出“肝硬化可逆”这一违反直觉的结论呢?编者认为存在以下几点原因:
1. 混淆“肝纤维化”与“肝硬化”的定义
很多的“宣传/科普”混淆了肝纤维化、肝硬化、肝硬化并发症的概念,或者说,故意偷换了概念。根据《中国肝硬化临床诊治共识意见》中的定义,假小叶形成是肝硬化的基本病理特点,也是确诊肝硬化最重要的病理依据。可以看出,肝硬化是一个病理诊断;作为肝脏慢性损伤连续过程的两个阶段,肝纤维化是肝硬化形成的必要阶段,肝硬化是肝纤维化发展的严重后果。因此,大多数研究的结论,患者肝纤维化等级的下降,并不能直接得出“肝硬化逆转”的结论。
2. 多数研究未达到肝硬化逆转的病理标准
《肝硬化诊治指南》(2019版)提出,肝纤维化/肝硬化逆转的标准为:Ishak评分纤维化分期降低≥Ⅰ期(病理逆转),或通过治疗后P-I-R分类下降。
(抛开这个并不是单纯肝硬化逆转标准的定义)我们先大致来了解下Ishak评分与P-I-R评分:
(1)Ishak评分系统将肝炎活动指数分为炎症、纤维化、脂肪变性、坏死四个主要类别,由经验丰富的病理医生对每个类别进行评分,相加得到的总分用来评估肝脏疾病的严重程度;
(2)PIR分型又称“北京标准”,也是基于肝脏穿刺活检的组织学评估,将治疗后的炎症活动度和纤维化程度与治疗前的结果进行对比,将患者分为不同的PIR类别。
可以看出肝纤维化/肝硬化逆转的标准需要肝穿刺的病理结果,而目前很多临床研究采用的无创检查指标如LSM、HVPG、FIB-4评分等,并不能完全反映肝纤维化/肝硬化等级是否下降。
3. 无创指标能否评价肝纤维化逆转仍有待验证
临床常用的无创评估肝纤维化/肝硬化的指标,包括LSM、FIB-4等。
肝脏硬度值(LSM):振动波在肝脏中的传播速度与肝脏的硬度成正比。因此,通过瞬时弹性成像技术测量波速,可以计算出肝脏的硬度值,以千帕(kPa)为单位表示。一般来说,LSM值越低,表示肝脏越柔软,纤维化程度越轻。但这种测量是间接反应肝纤维化程度,存在个体差异、操作差异、仪器差异、疾病影响等,具体的临界值可能因不同研究和地区而有所差异。
FIB-4是用于评估肝硬化风险的评分系统,公式为FIB-4 = (年龄 x 0.087) + (AST/ALT x 0.68) + (PLT x -0.13) + (ALB x -1.08)。分值越高表示肝硬化风险越高。一般认为FIB-4≥1.45表示肝硬化风险较高。但可以明显看出,公式中几项指标受治疗影响变异度较大,并不能完全反映肝硬化程度。
4. 偷换“肝硬化逆转”与“再代偿”概念
根据患者是否伴有EGV、出血、腹水、肝性脑病、黄疸等表现,肝硬化分为6期。
1期无静脉曲张和任何其他并发症;
2期出现静脉曲张,但无EGVB或腹水;
3期出现EGVB,但无腹水或肝性脑病等失代偿表现;
4期出现除EGVB以外的任意一项失代偿表现,包括腹水、显性肝性脑病、确定部位的细菌感染、非梗阻性黄疸等;
5期出现以上2种失代偿表现;
6期表现为反复发作的感染、肝外脏器功能障碍、慢加急性肝衰竭、顽固性腹水、持续性肝性脑病或黄疸。
1和2期患者无明显症状或并发症,为代偿期,5年病死率分别为1.5%和10%;3~5期患者出现EGVB、腹水和肝性脑病等并发症,为失代偿期,5年病死率分别为20%、30%、88%;6期为晚期失代偿期,1年病死率高达60%~80%。
肝硬化失代偿逆转(再代偿)是一个极为复杂的命题,既往的定义从韩国学者提出的“肝功能好转到CTP评分5分”,到中华医学会提出的“较长时间内(至少1年)不再出现肝硬化失代偿事件(腹水、消化道出血、肝性脑病等)”,再到BavenoⅦ共识的“病因控制、失代偿并发症消失和肝功能好转”。
但治疗过程中肝功能好转不代表病理结构逆转、门静脉高压缓解,经过病因治疗后重新代偿的疾病状态能否维持长期稳定而不再发生失代偿并发症尚不清楚。再代偿的机制仍处于探索中,需要从纤维化逆转、门静脉高压减轻、系统性炎症改善等方面进一步探讨相关的机制。
四、总结
总而言之,针对肝硬化的基本病理特点——“假小叶形成”,目前尚无明确证据证实可恢复为正常肝小叶的结构——即“肝硬化逆转”;但现阶段大量研究已发现,针对肝硬化的各个阶段的治疗,是可以在一定程度上减少肝损伤、降解纤维化、阻止结构紊乱、恢复再代偿,这无疑给广大的病友也带来了治疗信心。


