【协和医学杂志】STAR指南术语体系(三):报告、评价、传播、实施、更新
时间:2025-09-01 12:13:11 热度:37.1℃ 作者:网络
指南科学性、透明性和适用性评级工具(STAR)工作组方法与技术专业委员会于2025年初推出临床实践指南(下文简称“指南”)术语系列方法学文章,旨在构建覆盖指南制订全流程的术语理论框架。前期已为读者介绍了指南规划与启动阶段、证据评价与推荐意见形成阶段的50条术语[1-2],本文将聚焦指南生命周期中证据合成之后的关键环节,包括指南的报告、评价、传播、实施及更新。这些环节构成了连接证据转化与临床决策实践的核心桥梁,而其中所用的术语标准化程度直接决定了指南在临床环境中的有效应用。
术语标准化的重要性主要体现在以下方面:
1 提升信息保真度与清晰度。在指南的报告与撰写阶段,采用精准、规范的术语能够最大限度减少关键信息的失真或遗漏,并有效规避因术语歧义引发的临床误读风险。
2 增强评价的客观性与可比性。术语的一致性是确保指南质量评价客观、可靠的基础,可显著提升不同来源或不同版本指南在质量评价结果上的可比性,使得跨指南的优劣判断更为准确。
3 促进跨界传播与实施。在指南的跨国、跨语言及跨文化传播过程中,统一的术语体系能够有效抑制语义漂变(semantic drift)[3],保证核心概念的精准转译。同时,标准化的术语也为各国进行本土化适配提供了参照基准,从而有力推动指南在全球及特定区域内的有效传播、采纳与实施。
4 优化指南更新与迭代。术语的标准化有助于清晰标识和区分指南的不同更新版本,提高更新内容的可识别性与可追溯性。这不仅有助于指南使用者理解不同版本间的衍变,亦可间接促进指南更新方法学的规范化与推广应用。
尽管国内外学术机构和研究团队已发布多个指南制订/修订手册,但当前学术界对于指南的报告、评价、传播、实施及更新等阶段在指南制订全流程中的划分尚未完全统一,同时指南术语体系仍处于动态发展过程中,需兼顾规范性与灵活性。
因此,本文在《中国制订/修订临床诊疗指南的指导原则(2022版)》[4]的基础上,新增“其他”阶段,以补充现有指南术语体系。这一调整既遵循了指南术语标准化的要求,又体现了术语体系的前瞻性与包容性,以适应未来指南术语方法学的发展和完善。
1 资料与方法
1.1 检索策略
1.1.1指南制订手册的检索、术语的收集与遴选、术语释义的确定
本系列3篇文章关于“指南制订手册检索”“术语收集与遴选”“术语释义确定”的过程与原则一致,具体内容参见本系列首篇文章的方法学部分[1]。
1.1.2指南制订方法学文献的检索
本文主要纳入指南报告、评价、传播、实施及更新阶段的术语。中文检索词包括“指南”“方法”“评价”“传播”“实施”等,英文检索词包括“guideline*”“standard”“appraisal”“implementation”等。以PubMed为例,检索策略详见图1。

图1 PubMed检索策略
1.2 文献纳入与排除标准
本研究纳入指南制订手册或相关方法学研究中(包含指南报告、评价、传播、实施及更新阶段)的全部相关术语,研究发表语言限制为中文或英文;排除同一机构重复发表的文献以及无法获取全文的文献。
2 结果
2.1 检索结果与术语纳入情况
本研究最终纳入13部指南制订手册和32篇方法学文献。对相关指南术语进行提取、去重和标准化处理后,共识别出指南报告、评价、传播、实施及更新阶段相关术语30条。结合术语频次及团队经验,最终确定14条核心术语(表1)。
表1 指南报告、评价、传播、实施及更新阶段术语
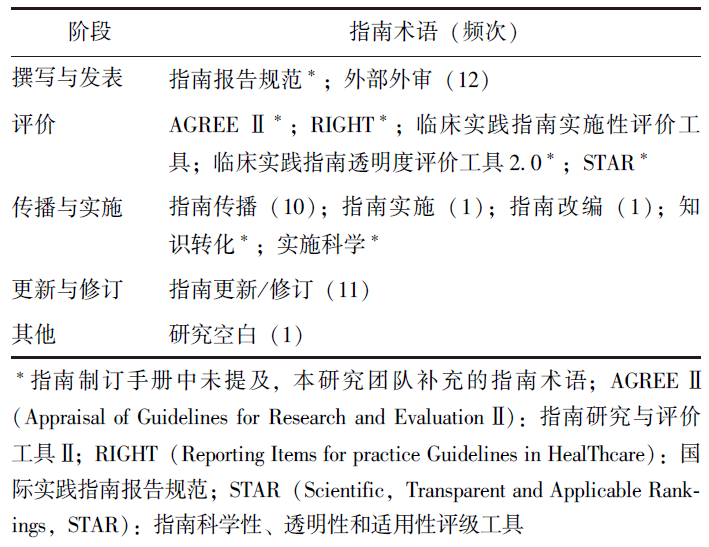
2.2 撰写与发表
2.2.1 指南报告规范
中文别称:指南报告清单
英文名称:reporting guidance for guideline;reporting checklist for guideline
释义:指南报告规范旨在为指南类文件提供撰写模板或标准,确保其结构完整、内容清晰、报告准确。这些规范通常以清单、流程图或文字说明等形式呈现,旨在指导指南制订者全面覆盖关键要素,并提升指南报告质量。
延伸介绍:目前主要的指南报告规范工具包括国际实践指南报告规范(RIGHT)、指南研究与评价工具(AGREE)报告清单、Check Up报告清单等,其中最常用的是RIGHT报告清单[4-7]。
2.2.2 外部审查
中文别称:指南外审
英文名称:external review of guideline
释义:外部审查是指将终版指南稿件送交未直接参与指南制订工作,且与指南不存在利益冲突的外部专家,从指南的方法学和临床内容及可读性等角度审查,针对指南存在的局限性或问题,给出反馈意见和建议。
延伸介绍:指南外审一般情况下不提出新的临床问题,也不增加或减少原有的推荐意见数量,而是对指南内容进行完善[8-11]。外审专家组成详见本系列文章《STAR指南术语体系(一):规划与启动》[1]。
2.3 指南评价
指南评价阶段的术语主要是针对指南方法学质量、报告质量、实施性、透明度、综合评级5个维度的评价工具,具体内容详见表2。
表2 指南评价工具及相关维度
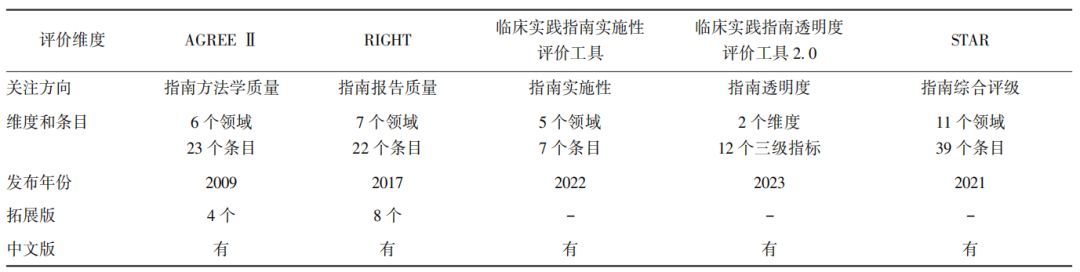
AGREE Ⅱ、RIGHT、STAR:同表1
2.3.1 AGREE Ⅱ
中文名称/别称:指南研究与评估系统/指南研究与评价工具Ⅱ
英文全称:Appraisal of Guidelines for Research and Evaluation Ⅱ
释义:AGREEⅡ是帮助指南制订者、使用者和研究者评估指南方法学质量,为指南制订提供方法学指导以及指导指南正确报告的工具。
延伸介绍:AGREE Ⅱ基于AGREE更新而来,包括范围和目的、参与人员、严谨性、清晰性、应用性、独立性6个领域共23个条目,可评估指南制订的方法学严谨性和透明度,并用于指导其开发过程。工作组目前已研发出针对外科干预(AGREE-S)、针对指南推荐意见评价(AGREE-REX)、针对卫生系统挑战(AGREE-HS)、精简版工具(AGREE-GRS)及AGREE-China等扩展版工具。读者可通过AGREE官网(https://www.agreetrust.org)获取工具、手册、翻译版、在线平台等相关资源[12-15]。
2.3.2 RIGHT
中文名称/别称:卫生保健实践指南的报告条目/国际实践指南报告规范
英文名称:Reporting Items for practice Guidelines in HealThcare
释义:RIGHT是常用的指南报告质量评价工具,可协助指南制订者、期刊编辑和卫生从业者评估指南全文信息报告的规范性和完整性,是否提供了足够细节供读者判断其可靠性,以及是否便于使用者理解和应用。
延伸介绍:该工具由中国学者牵头,联合12个国家及7个国际权威组织的30余名资深专家联合研发,涵盖基本信息、背景、证据、推荐意见、评审和质量保证、资助与利益冲突声明及管理、其他7个领域,共22个条目。目前工作组已完成针对改编版指南、患者版本指南、基层版本指南、针灸、中医药、中成药、利益冲突和资助、指南解读等8个扩展版工具的研发,以及6种语言的翻译。读者可在RIGHT官网(http://www.right-statement.org)查阅该工具条目、清单、解读、扩展板、翻译版及相关资源[16-17]。
2.3.3 临床实践指南实施性评价工具
英文名称:Implementation Evaluation Tool of Clinical Practice Guidelines
释义:临床实践指南实施性评价工具由临床医生和指南方法学专家共同对指南的可实施性进行评价,旨在从文本角度规范指南内容及形式的呈现,促进指南的实施,特别是规范指南推荐意见的撰写和设计实施策略,以促进对指南的全面评价,进而提高其推广与实施,其包括5个评价领域(可及性、沟通性、可执行性、易识别性和应用性),共7个评价条目[18]。
2.3.4 临床实践指南透明度评价工具2.0
英文名称:Transparency Evaluation Tool of Clinical Practice Guidelines 2.0
释义:临床实践指南透明度评价工具2.0通过对指南开发过程中受制订科学性和利益冲突管理有效性影响的决策依据、方法和利益冲突等信息进行评估,评价指南的透明度,目的是了解指南制订过程和利益冲突披露的真实性、完整性、充分性,包括利益冲突和制订流程2个维度,共12个三级指标[19-20]。
2.3.5 STAR
中文名称:指南科学性、透明性和适用性评级
英文名称:Scientific, Transparent and Applicable Rankings of Guideline
释义:STAR工具是由多学科专家团队研发,基于系统收集的多维度评价属性和条目,通过专家调查、层次分析法和专家共识等步骤形成指南综合评价工具,包括科学性、透明性和适用性3个维度,共11个领域、39个条目。
延伸介绍:STAR工作组通过研发STAR工具,旨在针对中国学者制定的指南和共识持续开展系统性评级工作,进一步帮助医务人员遴选和应用高质量指南。读者可访问STAR网站(https://www.star-guidelines.cn/)、关注“STAR指南”公众号了解评级条目详情、评级人员信息,查阅指南和共识STAR评分和评级规则等信息[21-24]。
2.4 传播与实施
2.4.1 指南传播
英文名称:guideline dissemination
释义:指南传播是指通过多种途径提高指南使用者对指南推荐意见的知晓和了解的过程[25-26]。
2.4.2 指南实施
英文名称:guideline implementation
释义:指南实施是实现指南从理论向实践转化,加速指南推广、应用并改变使用者行为的一系列过程,包括确定指南实施目标、制订指南实施计划、识别指南实施障碍、开发指南实施工具等[9,27-33]。
2.4.3 指南改编
英文名称:guideline adaption
释义:指南改编是根据特定地区、国家或医疗环境的需求,通过系统方法对已有指南的推荐意见进行修改以更好地符合当地实践要求的过程[31,34-40]。
2.4.4 知识转化
英文名称:knowledge translation
释义:知识转化属于转化医学(Translational Medicine)范畴,在循证医学领域是指将研究证据转化为临床实践和卫生政策的过程,旨在缩短研究与实践之间的差距,确保患者能够从最新的研究成果中获益[41-42]。
延伸介绍:指南是知识转化的一类。
2.4.5 实施科学
中文别称:实施性科学
英文名称:implementation science
释义:实施科学是研究如何将循证医学成果有效地应用于临床实践和卫生保健系统的学科,其关注如何克服实施障碍、促进研究成果采纳与持续应用,并最终改善医疗服务质量和健康结局。
延伸介绍:实施科学能够为指南实施提供系统的理论指导和方法学支持,促进指南在临床实践中得到有效应用和转化[43-46]。
2.5 更新与修订
中文名称:指南更新/修订
英文名称:guideline update;updating;revision
释义:指南更新/修订是指在指南发布后的一定时间内(通常为2~5年),因证据发生重要变化、卫生资源改变或其他使指南不适合继续指导临床实践等原因,遵循科学、规范的方法,对原有指南重新进行证据审查并更新推荐意见的过程[9-11,27,34-35,47-51]。
延伸介绍:指南更新/修订仍应基于系统评价的证据。
2.6 其他
中文名称:研究空白
英文名称:research gap
释义:研究空白是指在指南所关注的临床问题中,由于现有证据不足或质量低下,无法对某个或某些临床问题形成基于证据的推荐意见[52-53]。
延伸介绍:高质量指南一般会针对研究空白提出未来需进一步开展研究的建议。
3 讨论
工作组围绕指南的报告、评价、传播、实施及更新等环节,凝练并解释了14条相关术语,旨在协助指南制订者、评价者、研究者和使用者更好地理解和应用指南。
在指南完成制订工作与正式发表之前,具有两个至关重要的环节。
第一个环节是按照国际通用的报告清单或标准规范撰写指南。当前全球有600余个已经发表或正在制订的报告规范[54],其中用于指南的主要为RIGHT和AGREE报告清单。后者是AGREE工作组基于AGREE研发的报告清单,与RIGHT部分条目存在重叠,指南制订者在撰写指南时,可参考其中之一。若指南属于某个特殊类型(如专为针刺、中医药或患者制订的版本),对现有指南进行改编及更详细地呈现利益冲突等内容,RIGHT则提供了更为具体的扩展版。
第二个环节是指南外审。与其他类型的研究不同,在完成制订与投稿之前,指南制订者将邀请未直接参与指南制订的少数外部专家(主要是临床专家和方法学专家)对指南进行审核或小范围试用,以确保指南在制订流程上无重要疏漏,推荐意见易于理解,以及在临床应用过程中不会引起重大争议。通过外审收集专家反馈意见并进一步完善内容后,指南方可进行投稿。
投稿后,期刊编辑根据评审流程将指南送同行评审,因此指南类文稿将经历两次外审,而其他类型的研究则可能只经历一次外审。一方面,外审体现了指南相对于其他研究更加严格的质控要求;另一方面,对于不选择在期刊发表的指南尤为必要,如WHO、NICE等机构发布的指南,因各种原因不在期刊发表,此时外审是指南完善内容和质量的重要环节。
指南发表后,在应用于临床之前还应经过第三方独立评价。国际上通用的指南评价工具是AGREE,但其存在一定的局限性:(1)评价缺乏连续性和全面性,具体评价哪些领域、哪些年代的指南取决于研究人员的兴趣和时间;(2)评价人员代表性不足,评价者未经过严格培训,评价质量良莠不齐;(3)尽管评价结果在医学期刊发表,但很难直接影响到指南制订者。
2021年,STAR评级推出,每年对所有中国学者牵头制定的指南和共识类文献进行评级,并定期发布评级报告;同时所有参与评级的专家均接受统一培训和考核,合格后方可参与评级工作。STAR工作组搭建评级数据库,提供综合评分结果,举办指南评级研讨会,建立了40个专科评级委员会(大部分委员为中华医学会和中国医师协会的委员/会员),这些举措对于提升中国指南和共识质量发挥了重要作用。
此外,还需区分知识转化与实施科学之间的区别和联系。知识转化强调对医学知识进行及时、高效地传播和应用,指南即为其中一类知识。实施科学则强调采用一系列理论、框架和模型,对循证后确定安全、有效的结果进行实施,使其成为医学常规实践。指南实施是实施科学研究的重要内容之一。
最后,本文讨论了研究空白这一概念。一部高质量的指南,其功能不仅体现在对临床实践的指导,也体现在对未来研究的启发。在指南制订过程中,往往会发现某个或多个临床问题缺乏足够数量的证据或缺乏高质量的证据。此时,制订者应在指南正文的某一部分明确提出未来应优先开展的研究内容或选题,而这些研究则会进一步夯实证据基础,甚至改写指南推荐意见。
未来,随着指南方法学的不断进步,指南相关新术语将不断出现。本研究团队将积极关注该领域的发展,适时为读者梳理、总结和介绍指南术语相关概念和最新动态。
参考文献
[1]李哲玮, 史乾灵, 刘辉, 等. STAR指南术语体系(一): 规划与启动[J]. 协和医学杂志, 2025, 16(1): 216-223.
[2] 朱迪,李昊东,王子君,等.STAR指南术语体系(二):临床问题确定、证据检索与评价、推荐意见形成[J].协和医学杂志,2025,16(3):756-764.
[3]Beinborn L, Choenni R. Semantic drift in multilingual representations[J]. Comput Linguist, 2020, 46(3): 571-603.
[4]陈耀龙, 杨克虎, 王小钦, 等. 中国制订/修订临床诊疗指南的指导原则(2022版)[J]. 中华医学杂志, 2022, 102(10): 697-703.
[5]陈耀龙. 卫生保健实践指南的报告规范研究[D]. 兰州: 兰州大学, 2015.
[6]雷军强, 陈耀龙. 循证诊断学[M]. 北京: 北京大学医学出版社, 2023.
[7]彭晓霞, 方向华, 陈耀龙. 循证医学与临床研究[M]. 北京: 人民卫生出版社, 2019.
[8]Christensen R E, Yi M D, Kang B Y, et al. Development of an international glossary for clinical guidelines collaboration[J]. J Clin Epidemiol, 2023, 158: 84-91.
[9]National Health and Medical Research Council. Procedures and requirements for meeting the NHMRC standards for clinical practice guidelines[M/OL]. Melbourne: National Health and Medical Research Council, 2020[2025-02-15]. https://www.nhmrc.gov.au/sites/default/files/documents/reports/clinical%20guidelines/Procedures-and-requirements-for-meeting-the-2011-NHMRC-standard-for-clinical-practice-guidelines%2801%29.pdf.
[10]Scottish Intercolegiate Guidelines Network. SIGN50 A guideline developer's handbook[M]. Edinburgh: SIGN, 2019.
[11]Rosenfeld R M, Shiffman R N, Robertson P. Clinical Practice Guideline Development Manual, Third Edition: a quality-driven approach for translating evidence into action[J]. Otolaryngol Head Neck Surg, 2013, 148(S1): S1-S55.
[12]AGREE Collaboration. Development and validation of an international appraisal instrument for assessing the quality of clinical practice guidelines: the AGREE project[J]. Qual Saf Health Care, 2003, 12(1): 18-23.
[13]Brouwers M C, Kho M E, Browman G P, et al. AGREE II: advancing guideline development, reporting and evaluation in health care[J]. CMAJ, 2010, 182(18): E839-E842.
[14]Makarski J, Brouwers M C. The AGREE enterprise: a decade of advancing clinical practice guidelines[J]. Implement Sci, 2014, 9: 103.
[15]Brouwers M C, Spithoff K, Lavis J, et al. What to do with all the AGREEs? The AGREE portfolio of tools to support the guideline enterprise[J]. J Clin Epidemiol, 2020, 125: 191-197.
[16]Chen Y L, Yang K H, Maruic A, et al. A reporting tool for practice guidelines in health care: the RIGHT statement[J]. Ann Intern Med, 2017, 166(2): 128-132.
[17] RIGHT Working Group. RIGHT statement[EB/OL]. [2025-02-15]. https://www.right-statement.org/.
[18]靳英辉, 赵志慧, 黄粲然, 等. 临床实践指南实施性评价工具的研制和验证评价[J]. 中国循证医学杂志, 2022, 22(1): 111-119.
[19]张娜, 龙囿霖, 王心怡, 等. 临床实践指南透明度评价工具2.0的循证构建[J]. 中国循证医学杂志, 2023, 23(9): 1066-1071.
[20]杨柳, 龙囿霖, 程祎凡, 等. 临床实践指南透明度评价工具的循证构建[J]. 中国循证医学杂志, 2021, 21(8): 869-875.
[21]Yang N, Liu H, Zhao W, et al. Development of the scientific, transparent and applicable rankings (STAR) tool for clinical practice guidelines[J]. Chin Med J (Engl), 2023, 136(12): 1430-1438.
[22]Yang N, Wang X, He H, et al. Challenges and strategies for implementing the STAR tool for comprehensive evaluation of guidelines: A qualitative study with Chinese clinicians[J]. Chin Med J (Engl), 2024. doi: 10.1097/CM9.0000000000003384. Epub ahead of print.
[23]Yang N, Liu H, Estill J, et al. Enhancing clinical practice guidelines with STAR[J]. BMJ Evid Based Med,2025,30(3):212-213.
[24]孙雅佳, 史乾灵, 杨楠, 等. 临床实践指南综合评价的思考与探索[J]. 协和医学杂志, 2023, 14(1): 22-30.
[25]陈耀龙, 史乾灵, 赵俊强, 等. 从知到行: 跨越指南理论与实践的鸿沟[J]. 协和医学杂志, 2020, 11(6): 746-753.
[26]Frantsve-Hawley J, Rindal D B. Translational research: bringing science to the provider through guideline implementation[J]. Dent Clin North Am, 2019, 63(1): 129-144.
[27]GLOSS D. AES clinical practice guideline development manual[M/OL]. Chicago, IL: American Epilepsy Society, 2020[2025-02-15]. https://www.aesnet.org/docs/default-source/pdfs-clinical/aes_guideline_manual.pdf?sfvrsn=9a9ae64b_2.
[28]Papoutsakis C, Moloney L, Sinley R C, et al. Academy of nutrition and dietetics methodology for developing evidence-based nutrition practice guidelines[J]. J Acad Nutr Diet, 2017, 117(5): 794-804.
[29]Davino-Ramaya C, Krause L K, Robbins C W, et al. Transparency matters: Kaiser Permanente's National Guideline Program methodological processes[J]. Perm J, 2012, 16(1): 55-62.
[30]U.S. Preventive Services Task Force. U.S. preventive services task force procedure manual[EB/OL]. [2025-02-15]. https://www.uspreventiveservicestaskforce.org/uspstf/sites/default/files/2023-11/procedure-manual-2023.pdf.
[31]Ministry of Health of Saudi Arabia. Saudi Arabian handbook for healthcare guideline development[EB/OL]. [2025-02-15]. https://www.moh.gov.sa/en/Ministry/Structure/Programs/TCP/Documents/Saudi%20Arabian%20Handbook%20for%20Healthcare%20Guideine%20Development-updat-ed16-7.pdf.
[32]Gagliardi A R, Marshall C, Huckson S, et al. Developing a checklist for guideline implementation planning: review and synthesis of guideline development and implementation advice[J]. Implement Sci, 2015, 10: 19.
[33]赖鸿皓, 孙铭谣, 黄嘉杰, 等. 中西医结合临床实践指南实施框架构建的思考[J]. 协和医学杂志, 2023, 14(1): 31-38.
[34]Weimer M B, Devoto A, Kansagara D, et al. The American Society of Addiction Medicine clinical practice guideline development methodology[J]. J Addict Med, 2024, 18(4): 366-372.
[35]WHO. Estonian handbook for guidelines development 2020[EB/OL]. [2025-02-15]. https://ravijuhend.ee/uploads/userifles/Estonian_Handbook_for_Guidelines_Development_2020_copy.pdf.
[36]THE ADAPTE Collaboration. The ADAPTE process:resource toolkit for guideline adaptation[EB/OL]. [2025-02-15]. https://g-i-n.net/wp-content/uploads/2021/03/ADAPTE-Resource-toolkit-March-2010.pdf.
[37]胡晶, 陈茹, 谢雁鸣, 等. 科学和规范的改编临床实践指南[J]. 中国循证儿科杂志, 2012, 7(3): 226-230.
[38]Mehndiratta A, Sharma S, Gupta N P, et al. Adapting clinical guidelines in India-a pragmatic approach[J]. BMJ, 2017, 359: j5147.
[39]McCaul M, Ernstzen D, Temmingh H, et al. Clinical practice guideline adaptation methods in resource-constrained settings: four case studies from South Africa[J]. BMJ Evid Based Med, 2020, 25(6): 193-198.
[40]陈耀龙, 张先卓, 周奇, 等. 临床实践指南的改编[J]. 协和医学杂志, 2020, 11(1): 102-108.
[41]Davis D, Evans M, Jadad A, et al. The case for knowledge translation: shortening the journey from evidence to effect[J]. BMJ, 2003, 327(7405): 33-35.
[42]Canadian Institutes of Health Research. Guide to knowledge translation planning at CIHR: integrated and end-of-grant approaches[M]. Ottawa: Canadian Institutes of Health Research, 2012.
[43]徐东, 陈江芸, 蔡毅媛. 实施科学的前世今生(上篇):起源与发展[J]. 协和医学杂志, 2024, 15(2): 442-449.
[44]National Institute of Health. Implementation science news, resources and funding for global health researchers[EB/OL]. [2024-02-16]. https://www.fic.nih.gov/researchtopics/pages/implementationscience.aspx.
[45]Eccles M P, Mittman B S. Welcome to implementation science[J]. Implement Sci, 2006, 1(1): 1.
[46]Peters D H, Tran N T, Adam T. Implementation research in health: a practice guide[M]. Geneva: World Health Organization, 2013.
[47]Mohd Mustapa M F, Exton L S, Bell H K, et al. Updated guidance for writing a British Association of Dermatologists clinical guideline: the adoption of the GRADE methodology 2016[J]. Br J Dermatol, 2017, 176(1): 44-51.
[48]Qaseem A, Kansagara D, Lin J S, et al. The development of clinical guidelines and guidance statements by the clinical guidelines committee of the American College of Physicians: update of methods[J]. Ann Intern Med, 2019, 170(12): 863-870.
[49]Becker M, Neugebauer E A M, Eikermann M. Partial updating of clinical practice guidelines often makes more sense than full updating: a systematic review on methods and the development of an updating procedure[J]. J Clin Epidemiol, 2014, 67(1): 33-45.
[50]Vernooij R W M, Alonso-Coello P, Brouwers M, et al. Reporting items for updated clinical guidelines: checklist for the reporting of updated guidelines (CheckUp)[J]. PLoS Med, 2017, 14(1): e1002207.
[51]陈耀龙, 王玲, 杨楠, 等. 临床实践指南如何 “保鲜”[J]. 协和医学杂志, 2020, 11(2): 207-212.
[52]Wang Q, Wang X Q, Chen Y L, et al. Research gap of guidelines might be an important approach to prioritization (Letter commenting on: J Clin Epidemiol. 2015;68:341-6)[J]. J Clin Epidemiol, 2016, 69: 251-252.
[53]Robinson K A, Saldanha I J, Mckoy N A. Frameworks for determining research gaps during systematic reviews: Report No.:11-EHC043-EF[R]. Rockville: Agency for Healthcare Research and Quality, 2011.
[54]Equator Network. Enhancing the quality and transparency of health research[EB/OL]. [2025-02-15]. https://www.equator-network.org/.


